Hauptgruppenelemente: Club der Dreifachbindungen bekommt neues Mitglied

Deutsche Wissenschaftler haben eine Lücke in der Chemie der Hauptgruppenelemente geschlossen: Sie stellten ein Molekül her, das eine bisher nur theoretisch vorhergesagte echte Dreifachbindung zwischen zwei Boratomen enthält. Neben Kohlenstoff und Stickstoff ist Bor erst das dritte Element, von dem dieser Bindungstyp bekannt ist. Um das zu erreichen stabilisierte das Team um Holger Braunschweig von der Universität Würzburg die beiden Boratome mit N-Heterozyklischen Carbenen, die sehr elektronenreich sind und daher die Elektronen des Bor in die ungeliebte Dreifachbindung zwingen.
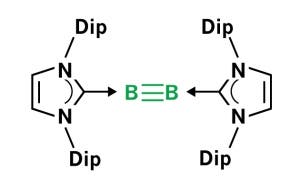
Hinweise darauf, dass dieser Typ von Bindung auch beim Bor möglich sein sollte, gab es schon lange: Bor besitzt drei Valenzelektronen, die je eine Bindung eingehen können. Direkt nebenan im Periodensystem liegen außerdem Stickstoff und Kohlenstoff, die ebenfalls drei und vier Valenzelektronen übrig haben – und beide bilden stabile Dreifachbindungen aus. Auch theoretische Rechnungen zeigten, dass Moleküle mit einer Dreifachbindung zwischen zwei Boratomen stabil sein sollten.
Ein solches Molekül in der Praxis herzustellen gestaltete sich jedoch schwierig. Zweiatomiges Bor mit Dreifachbindung existiert, anders als beim Stickstoff, nicht – das Molekül muss durch elektronenreiche Liganden an beiden Enden stabilisiert werden. Ein erster Teilerfolg gelang Forschern 2002, die zweiatomiges Bor mit Kohlenmonoxid stabilisierten, das allerdings nur für kurze Zeit und bei extrem niedrigen Temperaturen. Auch die Stabilisierung mit einem N-Heterozyklischen Carben hatten Forscher zuvor bereits ausprobiert, waren aber daran gescheitert, dass die Zwischenprodukte der Kopplung der beiden Boratome unerwünschte Nebenreaktionen eingehen. Erst Braunschweig und Kollegen lösten das Problem, indem sie einen Ausgangsstoff wählten, in dem die Boratome schon miteinander verbunden sind. Das entstehende Molekül zersetzt sich erst bei Temperaturen weit über 200 Grad Celsius.






Schreiben Sie uns!
1 Beitrag anzeigen