Lexikon der Biochemie: Fusicoccin
Fusicoccin, Fusicoccin A (Abb. 1), das Haupttoxin aus Kulturfiltraten von Fusicoccum amygdali, einem pathogenen Pilz, der für eine Welkkrankheit von Mandel und Pfirsich verantwortlich ist. Man nimmt an, dass F. ein einziges zentrales Transportsystem spezifisch aktiviert (möglicherweise durch Wechselwirkung mit der Plasmalemma-ATPase, wodurch die Umwandlung von Phosphatbindungsenergie in Protonengradientenenergie stimuliert wird) und dass alle anderen Effekte des Toxins Folgen dieses fundamentalen Vorgangs sind. Bei höheren Pflanzen ruft F. im Allgemeinen Zellvergrößerung, Protonenfluss, K+-Fluss und Stomataöffnung hervor. Es fördert auch die Samenreifung in Antagonismus zu Abscisinsäure.
Man unterscheidet zwei Reihen verwandter F., die alle als Cometabolite im Kulturfiltrat von Fusicoccum amygdali vorkommen: F. A und zehn Cometabolite, die sich nur in Anzahl und Position von Acetylgruppen unterscheiden (verursacht möglicherweise durch nichtenzymatische in-vitro-Wanderung von Acetylgruppen) sowie zwei 19-Desoxyfusicoccine.
Markierungsexperimente zeigen, dass die F. Diterpene sind (die strukturell ähnlichen Ophiobolane sind Sesterterpene). Drei von vier möglichen 4-pro-R-Wasserstoffatomen der Mevalonsäure werden in das Aglycon inkorporiert, davon eines an C6 und eines an C15, jedoch keines an C3. Eines der H-Atome an Position 2 der Mevalonsäure wird in C8 eingebaut (bei Ophiobolin wandert dieser Wasserstoff zu C15). Sechs von acht möglichen Wasserstoffatomen in Position 5 der Mevalonsäure werden in das Aglycon inkorporiert, zwei von ihnen an C9 und C13. Zusammen mit den Markierungsmustern von 13C- und 14C-markierter Mevalonsäure sind diese Resultate nur mit einer Synthese über all-trans-Geranylgeranylpyrophosphat konsistent (Abb. 2). Der abschließende Ringschluss durch zwei aufeinanderfolgende 1,2-Hydridverschiebungen wurde mit Hilfe des Einbaus von [3-13C,4-2H2]-(3RS)-Mevalonlacton gezeigt. Die NMR-Analyse des gebildeten F. ergab, dass die Signale, die durch 13C7 und 13C15 hervorgerufen werden, durch die Gegenwart von 2H an jedem von ihnen stark abgeflacht werden.
Die F. und Cotylenine bilden eine Verbindungsklasse, von denen keine weiteren natürlich vorkommenden Repräsentanten bekannt sind. Der glycosidische Zuckerrest ist ebenfalls ungewöhnlich für Fungusmetabolite. [E. Marre Annu. Rev. Plant Physiol. 30 (1979) 273-278 (Wirkungsweise und Physiologie); A. Banerji et al. J. Chem. Soc. Chem. Comm. (1978) 843-845 (Biosynthese)]
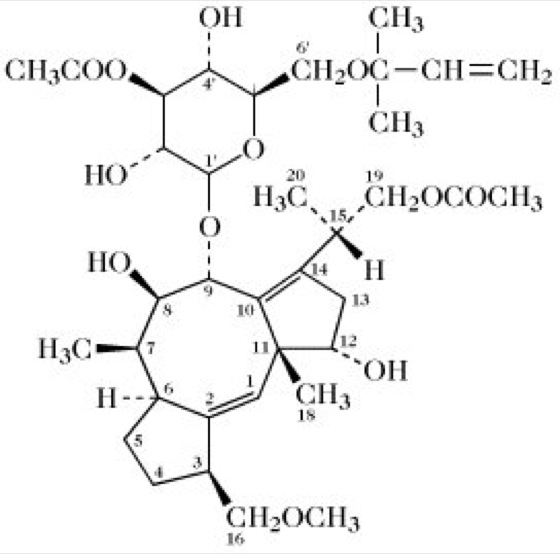
Abb. 1. Fusicoccin [K.D. Barrow et al. Chem. Commun. 19 (1968) 1.198-1.200]
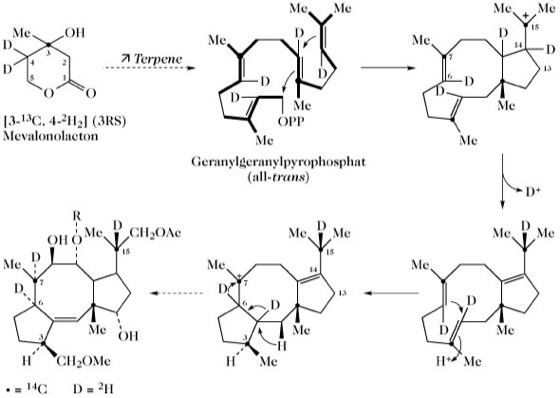
Abb. 2. Fusicoccin. Biosynthese des Aglyconrings der Fusicoccine.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.