Lexikon der Biologie: Allosterie
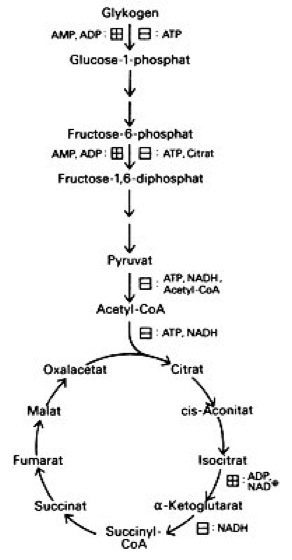
Allosteriew [von *allo –, griech. stereos = fest; Adj. allosterisch], Eigenschaft vieler aus mehreren Untereinheiten zusammengesetzter Proteine, in mehr als einer – häufig zwei – stabilen Konformation der Gesamtstruktur vorzukommen. Proteine dieser Eigenschaft werden allosterische Proteine genannt. Die Umwandlung von einer zur anderen Konformation wird als allosterische Umwandlung oder allosterischer-Effekt bezeichnet. Sie wird durch niedermolekulare Stoffe (allosterische Effektoren) bewirkt, die im Fall von allosterisch regulierten Enzymen(allosterische Enzyme) nicht identisch mit Substratmolekülen (Substrat) sind und die an anderen Stellen der Enzymstruktur als die Substratmoleküle, also nicht im aktiven Zentrum, binden. Obwohl die Bindungen der Effektoren nicht im aktiven Zentrum erfolgen, können die mit der Effektorbindung einhergehenden Konformationsänderungen eine Aktivierung oder eine Inaktivierung des aktiven Zentrums und damit eine Aktivierung bzw. Hemmung der betreffenden Enzyme, Transportproteine, Regulatorproteine usw. bewirken. Die Aktivierung eines allosterischen Proteins durch einen allosterischen Effektor wird als allosterische Aktivierung oder positiver allosterischer Effekt bezeichnet. Demgegenüber nennt man die Hemmung eines allosterischen Proteins durch einen allosterischen Effektor allosterische Hemmung (vgl. Abb.) oder negativen allosterischen Effekt. Die Bindestelle eines allosterischen Proteins für das Effektormolekül wird als allosterisches Zentrum (im Gegensatz zum aktiven Zentrum, der Bindestelle für Substrate) bezeichnet. – Allgemein können mit Hilfe allosterischer Effekte die Aktivitäten von Proteinen (katalytische Aktivitäten von Enzymen, Bindeaktivitäten von Transportproteinen oder Regulatorproteinen) durch Kleinmoleküle reguliert werden, die stereochemisch (Stereochemie) nicht mit den entsprechenden Substratmolekülen und damit auch nicht mit den entsprechenden aktiven Zentren der betreffenden Proteine verwandt sind. Allosterisch regulierte Proteine sind daher im Stoffwechsel der Zelle weit verbreitet und von großer Bedeutung. Häufig katalysieren allosterische Enzyme den ersten Schritt einer Biosynthesekette (Biosynthesewege) und werden durch das Endprodukt der betreffenden Biosynthesekette allosterisch inhibiert (allosterischeEndprodukthemmung). So wird z. B. bei der Biosynthese der aromatischen Aminosäuren die Aktivität von Chorismatmutase durch Phenylalanin bzw. Tyrosin allosterisch gehemmt (vgl. Abb.). Ebenso wird Aspartat-Transcarbamylase, das erste Enzym der Pyrimidinnucleotidsynthese, durch das Endprodukt Cytidintriphosphat gehemmt (vgl. Abb.). Endprodukte paralleler Stoffwechselwege (z. B. Tryptophan bei Chorismatmutase) können dieser Hemmung entgegenwirken, indem sie als positive allosterische Effektoren die entsprechenden Enzymaktivitäten stimulieren. Weitere Beispiele allosterischer Regulation von Enzymaktivitäten finden sich im Energiestoffwechsel ( vgl. Abb. ), wobei außer dem ersten Schritt auch Folgeschritte reguliert werden und an zwei Stellen antagonistische Wirkung zwischen AMP (Adenosinmonophosphat) und ADP (Adenosin-5´-diphosphat) einerseits und ATP (Adenosintriphosphat) andererseits beobachtet wird. Ein durch Sauerstoffbindung an Hämoglobin induzierter allosterischer Effekt liegt dem Bohr-Effekt zugrunde und dokumentiert die Bedeutung der Allosterie für Transportproteine (Membran, Membrantransport). Auch bei Membranproteinen, z. B. bei Adenylat-Cyclase, konnten allosterische Umwandlungen beobachtet werden. Bei der Regulation von Genaktivitäten (Genregulation) unterliegt die Bindestärke von Regulatorproteinen (Repressoren bzw. Aktivatoren) an die entsprechenden DNA-Signalstrukturen (Operatoren, Cap-Bindestellen) einer allosterischen Regulation (Genregulation). – Gegensatz von Allosterie ist die Isosterie. Beispielsweise wird bei isosterischer Enzymhemmung die Bindung von Substratmolekülen direkt im aktiven Zentrum durch Kompetition mit Molekülen, die dem Substrat ähnlich sind – oft mit dem Reaktionsprodukt –, gehemmt (kompetitive Hemmung, Produkthemmung). Biosynthesewege, Feedback, Monod (J.L.).
H.K.
| |
Abb. links: Schematische Darstellung der allosterischen Endprodukthemmung (Feedback-Regulation). Das erste Enzym einer Reaktionskette, ein allosterisches Enzym, wird von dem Endprodukt der gesamten Reaktionskette gehemmt. Abb. rechts: Ein Beispiel für eine allosterische Endprodukthemmung ist die Bildung von Cytidintriphosphat (CTP), das aus Carbamylphosphat und Aspartat über eine Reihe von Reaktionsschritten entsteht. Das erste an seiner Synthese beteiligte Enzym, die Aspartat-Transcarbamylase, ist ein allosterisches Enzym, das durch CTP, also das Endprodukt des ganzen Reaktionsweges, gehemmt wird. | |
 |


Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.