Lexikon der Chemie: elektrostatische Scheidung
elektrostatische Scheidung, die Trennung von Mineralgemischen in die Einzelkomponenten im elektrischen Feld. Durch Unterschiede in der Oberflächenleitfähigkeit, im Kornübergangswiderstand oder durch verschiedene Dielektrizitätskonstanten werden Teilchen, die in ein elektrisches Feld eingeführt werden, verschieden stark von ihrer ursprünglichen Bewegungsrichtung abgelenkt und können getrennt aufgefangen werden. Man unterscheidet bei der e. S. zwischen 1) Starkfeldscheidung, bei der im Sprühfeld Ionisation durch Koronaeffekte auftritt, wobei die Trennung durch Unterschiede in der Oberflächenleitfähigkeit erfolgt, und 2) Schwachfeldscheidung in einem Kondensatorfeld durch unterschiedliche Dielektrizitätskonstanten. Die e. S. kann im elektrostatischen Kammer- oder Walzenscheider erfolgen (Abb.). Dabei werden die Teilchen im elektrischen Feld polarisiert. Beim Verlassen des elektrischen Feldes verlieren die gut leitenden Teilchen ihr durch die Polarisierung erhaltenes Dipolmoment sofort und fallen infolge der Schwerkraft von der Walze. Die Teilchen mit der schlechteren Leitfähigkeit behalten ihr Dipolmoment und bleiben weiter an der Walze haften. Voraussetzung für die e. S. ist ein geringer Wassergehalt des Materials, weil die Oberflächenfeuchtigkeit die Unterschiede in der Oberflächenleitfähigkeit praktisch aufhebt.
Die e. S. wird bei der Aufbereitung von Kali- und Steinsalz, Eisenerzen, Schwermineralsanden zur Gewinnung von Diamanten aus Sanden und zur Trennung von Kunststoffen angewendet.
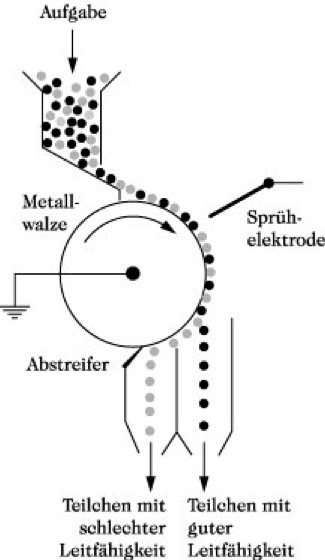
elektrostatische Scheidung. Abb.: Walzenscheider.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.