Lexikon der Chemie: Fluorwasserstoff
Fluorwasserstoff, HF, farblose, leicht bewegliche, giftige, ätzende (Flußsäure), an der Luft rauchende Flüssigkeit; D. (am Kp.) 0,991 g cm-3, F. -83,55 °C, Kp. +19,51 °C; krit. Temp. +230,2 °C. F. zeigt eine ausgeprägte Neigung zur Assoziation durch Ausbildung von Wasserstoffbrücken. Im kristallinen Zustand liegen lange Zick-Zack-Ketten vor (Abb.); die Assoziation des F. auch in flüssiger Phase bedingt dessen auffallend hohen Schmelz- und Siedepunkt. In der Dampfphase, nahe am Siedepunkt, liegt ein temperatur- und druckabhängiges Gleichgewicht zwischen hexameren (HF)6- und monomeren HF-Molekülen vor, erst bei 90 °C ist F. monomolekular. F. zählt neben N2 und CO zu den stabilsten bekannten zweiatomigen Molekülen. Flüssiger F. ist ein vorzügliches, wasserähnliches Lösungsmittel, das gemäß 3 HF ![]()
H2F+ + HF-2 einer gewissen Eigendissoziation unterliegt (Ionenprodukt = 10-11). Mit Wasser ist F. in allen Verhältnissen mischbar (Flußsäure). Er kommt mit einer Reinheit von ≈ 99,5 % in den Handel. Man verwendet F. vor allem zur Herstellung der als Aerosole dienenden Fluorkohlenwasserstoffe, von Metallfluoriden, wie Uran(IV)- oder Chrom(III)-fluorid, und von Ammoniumhydrogenfluorid sowie von Fluoroschwefelsäure. Er dient weiterhin als Solvens im chem. Laboratorium.
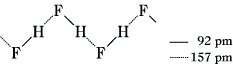
Fluorwasserstoff. Abb.: Assoziation des Fluorwasserstoffs.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.