Lexikon der Chemie: Naphthole
Naphthole, Hydroxynaphthaline, Derivate des Naphthalins, bei denen ein, zwei oder auch mehrere H-Atome durch Hydroxygruppen -OH substituiert sind. Die N. ähneln in ihren chemischen Eigenschaften den Phenolen, jedoch sind sie meist reaktionsfähiger. Sie sind schwer löslich in kaltem Wasser, etwas leichter in heißem Wasser und sehr leicht in Ethanol, Ether, Benzol und wäßriger Natronlauge. Wichtigste Verbindungen sind Naphth-1-ol und Naphth-2-ol, die in geringen Mengen im Steinkohlenteer vorkommen.
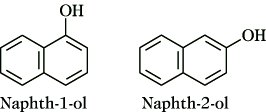
Naphth-1-ol (α-Naphthol, 1-Hydroxynaphthalin), farblose, leicht sublimierbare Kristallnadeln mit phenolartigem Geruch; F. 96 °C, Kp. 288 °C. Mit Eisen(III)-chlorid gibt Naphth-1-ol eine violette Farbreaktion.
Naphth-1-ol läßt sich leicht in 4-Stellung elektrophil substituieren oder mit Chrom(VI)-oxid zu 1,4-Naphthochinon oxidieren. Die Herstellung von Naphth-1-ol erfolgt entweder durch Sulfonierung von Naphthalin in 1-Position und Alkalischmelze der Naphthalin-1-sulfonsäure oder durch Behandlung von 1-Naphthylamin mit verd. Schwefelsäure bei 180 °C. Verwendet wird Naphth-1-ol vor allem zur Herstellung von Azofarbstoffen.
Naphth-2-ol (β-Naphthol, 2-Hydroxynaphthalin), farblose, rautenförmige Kristalle, die beim Sublimieren Blättchen ergeben; F. 123 °C, Kp. 295 °C. In verd. Lösung gibt es mit Eisen(III)-chlorid eine grüne Farbreaktion. Die Herstellung von Naphth-2-ol erfolgt durch Sulfonierung von Naphthalin in 2-Stellung (bei 165 °C) und nachfolgender Alkalischmelze. Naphth-2-ol ist reaktionsfähiger als die isomere 1-Verbindung und hat große Bedeutung zur Herstellung von Azofarbstoffen, als Ausgangsstoff zur Synthese von Insektiziden und Fungiziden sowie als Konservierungsmittel. Einige seiner Ether, z. B. Nerolin, sind wertvolle Riechstoffkomponenten.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.