Lexikon der Chemie: phosphorige Säure
phosphorige Säure, H3PO3, farblose, hygroskopische, wasserlösliche Kristalle; D. 1,651 g cm-3, F. 73,6 °C, Z. 200°C. Die Derivate der p. S. leiten sich von zwei tautomeren Formen ab.
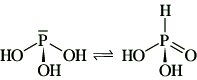
Die freie Säure und die einfachen Salze enthalten tetraedrische Anionen mit einem unmittelbar an den Phosphor gebundenen Wasserstoffatom. Entsprechend ist die Säure nur zweibasig und bildet zwei Reihen von Salzen, primäre und sekundäre Phosphite. Dagegen lassen sich Ester von beiden Formen ableiten. Beim Erhitzen der p. S. erfolgt Disproportionierung zu Phosphorsäure und Phosphin: 4 H3PO3 → 3 H3PO4 + PH3. Man gewinnt p. S. durch Hydrolyse von Phosphortrichlorid: PCl3 + 3 H2O → H3PO3 + 3 HCl.
Copyright 1998 Spektrum Akademischer Verlag, Heidelberg
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.