News: Verdünntes Quecksilber
Es ist allerdings knifflig, die Verbindung auf ihrem Weg durch das Nahrungsnetz zu verfolgen. Die Konzentrationen in der Umwelt – insbesondere in Seen – sind so gering, dass sie an der Nachweisgrenze liegen. Rätselhaft blieb außerdem, warum sich die Gehalte in Fischen und anderen Tieren je nach Jahreszeit unterscheiden. Paul Pickhardt vom Dartmouth College und seine Kollegen fragten sich daher, ob womöglich das schwankende Nahrungsangebot an der Basis, also auf Ebene des Phytoplanktons, bereits die spätere Verbreitung des Stoffes beeinflussen könnte.
In großen Tanks, so genannten Mesokosmen, bildeten sie einfache Süßwassersystem nach, in denen sie das Nährstoffangebot staffeln konnten. Je nach Ernährungslage blühte die eingesetzte Algenpopulation mehr oder weniger umfangreich. Dann setzten die Forscher anorganisches Quecksilber und Methylquecksilber zu, wobei sie für die Probenansätze unterschiedliche Quecksilber-Isotope verwendeten. So konnten sie das weitere Schicksal des Schwermetalls verfolgen.
24 Stunden später kontrollierten die Wissenschaftler die Quecksilbergehalte in den Algen. Es zeigte sich ein deutlicher Verdünnungseffekt: Je größer die Algen-Biomasse, desto geringer war die Metallkonzentration in den einzelnen Zellen.
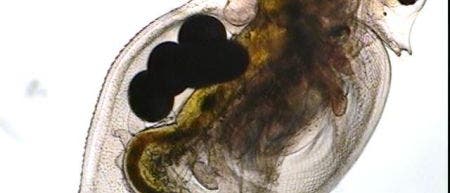
Im nächsten Schritt fügten Pickhardt und seine Mitarbeiter nun Wasserflöhe (Daphnien) hinzu – Zooplankton, das sich von Algen ernährt. Zwei und drei Wochen später bestimmten die Forscher erneut die Quecksilberkonzentrationen im Wasser, den Algen und den Daphnien. Und wie erwartet, lagen die Werte durchaus weit auseinander. In den Behältern mit hohem Nährstoffangebot und damit reichlicher Algenblüte waren die Wasserflöhe erheblich weniger mit Quecksilber belastet als in den nährstoffarmen Tanks – die geringere Vorbelastung ihres pflanzlichen Futters verschonte sie.
Wobei es allerdings auf die jeweilige Quecksilberquelle ankam. Denn die Abhängigkeit von der Nährstoffversorgung zeigte sich nur bei Methylquecksilber, die Aufnahme des anorganischen Quecksilber-Isotops blieb davon unbeeinflusst. Das sei jedoch nicht weiter verwunderlich, erklären die Forscher. Denn während das Methylquecksilber in die Algen eindringt und so auf jeden Fall aufgenommen wird, bleibt das anorganische Quecksilber "außen vor": Es lagert sich nur an der Außenseite an und wird daher nicht unbedingt aufgenommen.
Da im Jahresverlauf die Algenkonzentrationen in Seen stark schwanken – insbesondere, wenn die Gewässer mit Nährstoffen überlastet, also eutrophiert sind –, verändert sich damit auch die Gefahr der Quecksilberaufnahme in der anschließenden Nahrungskette. Ein Aspekt, der wichtig ist, sobald es um die Verabschiedung von Grenz- oder Richtwerten geht. Denn eine Forelle im April ist dann etwas ganz anderes als im Juli oder Oktober.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.