Lexikon der Arzneipflanzen und Drogen: Alkaloide
Alkaloide
stickstoffhaltige, meist basisch reagierende und vorwiegend heterocyclische Naturstoffe vgl. Formel Pyridin, Piperidin, Chinolin, Isochinolin, Chinolizidin, Chinazolin, Pyrrolidin, Pyrrolizidin, Imidazol, Indol, Carbonin, Tropan, Purin, Phenanthren, Aporphin. Sie sind meist pflanzlichen Ursprungs und besitzen oft charakteristische Wirkungen auf den tierischen und menschlichen Organismus. Ihre biogenetischen Vorstufen sind überwiegend Aminosäuren, wobei cyclische Aminosäuren (Phenylalanin, Tyrosin und Tryptophan) dominieren. Gegenüber den sog. "echten Alkaloiden" werden mitunter Verbindungen, deren N-Atom nicht in einen Heterocyclus integriert ist, z.B. Ephedrin, als Protoalkaloide, und diejenigen, die nicht aus Aminosäuren hervorgegangen sind, z.B. Terpen- und Steroidalkaloide, als Pseudoalkaloide bezeichnet. Viele A. tragen Trivialnamen. Sie enden stets auf der Endung "in" und wurden oft nach ihrer botanischen Herkunft, z.B. Atropin (Atropabelladonna), und Chelidonin (Chelidonium majus), z.T. nach ihrer Wirkung, z.B. Emetin (Emetikum) und in Ausnahmefällen auch nach bedeutenden Alkaloidchemikern, z.B. Pelletierin (Apotheker P. J. Pelletier, 1788-1842) benannt. In der Pflanze liegen die A. meist als Gemische vor. Fast immer dominiert eine Verbindung; diese bezeichnet man als Hauptalkaloid, die übrigen als Nebenalkaloide. Letztere sind meist Variationen des Hauptalkaloids, die sich in Art, Stellung oder Zahl der Substituenten, mitunter auch durch die Lage der Doppelbindung unterscheiden. Sie werden oft durch Anhängen eines Suffixes vom Hauptalkaloid unterschieden, z.B. Hydrastin → Hydrastinin, durch Voranstellen eines Präfixes, z.B. Berberin → Protoberberin oder durch vom Hauptalkaloid abweichende Buchstabenmodifikationen, z.B. Narcotin → Cotarnin. Isomere A. bezeichnet man oft mit Präfixen, u.a. Iso-, Pseudo- und Epi- oder durch Symbole, wie α-, β-, γ- usw. Verbindungen, denen die N-Methylgruppe fehlt, wird das Präfix "Nor" vorangestellt, z.B. Ephedrin → Nor-Ephedrin. A. sind fast ausnahmslos lipophile Verbindungen. Sie bilden mit Säuren Salze, die meist wasserlöslich sind. Auch in der Pflanze liegen sie gewöhnlich als Salze organischer Pflanzensäuren, u.a. Essig-, Äpfel- oder Weinsäure, vor. Sowohl die Basen als auch die Salze sind meist farblos und fest. Ausnahmen bilden hierbei u.a. das gelbgefärbte Berberin und das Protopin. A. bestehen i.d.R. aus den Elementen C, H, N und O. Nur wenige A. sind sauerstofffrei; diese sind alle flüssig, z.B. Coniin, Nicotin und Spartein. Die Einteilung der A. erfolgt nach ihrem heterocyclischen Ringsystem. Aufgrund ihrer oft starken physiologischen Wirkung, ihrer Wechselwirkungen mit post- und praesynaptischen Rezeptoren, Enzymen und Ionenkanälen, stellen viele A. wichtige biogene Arzneistoffe, z.T. auch gefährliche Giftstoffe, dar. Ihre Besprechung erfolgt an den gesonderten Stellen bei den Einzelverbindungen.
Histor.: Den Namen Alkaloid prägte im Jahre 1819 der Apotheker W. Meissner in Halle im Zusammenhang mit der Entdeckung des Veratrins. Meissner forderte, die bekannten alkalischen Pflanzenstoffe nicht mit den Namen Alkalien zu belegen, da sie von diesen in ihren Eigenschaften abweichen.
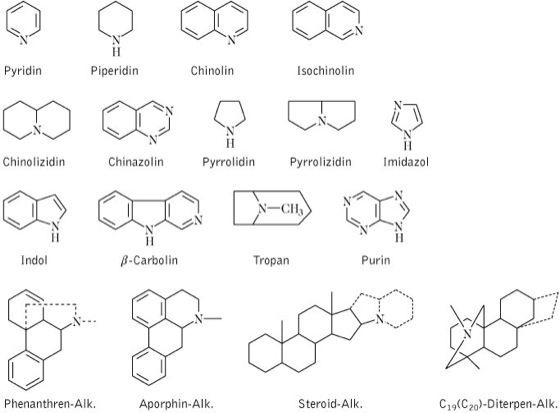
Alkaloide: Heterocyclische Grundkörper der Alkaloide.





Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.