Kryosphäre: Noch kein Gespür für Schnee

Eis gilt als zentraler Faktor für das Klima, die Geologie und das Leben. Um vorhersagen zu können, wie sich unser Planet zukünftig entwickelt und um zu enträtseln, wie das Leben im Universum entstand, muss man sein Verhalten verstehen. Gefrorenes Wasser überzieht Planeten, Monde und Kometen in unserem Sonnensystem. Auf der Erde reflektieren die Eiskappen bis zu 90 Prozent der einfallenden Sonnenstrahlung. Durchschnittlich bedeckt Eis etwa sieben Prozent der Meeresoberfläche, es beeinflusst ozeanische Strömungen und beschränkt den Gasaustausch von Atmosphäre und Wasser. Schnee und Eis hüllen ständig rund zehn Prozent der Erdoberfläche ein – und bis zur Hälfte der Nordhalbkugel während des dortigen Winters. Diese Decke aus gefrorenem Wasser dämmt Festland wie Ozeane.
Und das ist noch lange nicht alles: Eiswolken konzentrieren aufsteigende Chemikalien und bilden die Grundlage für atmosphärische Reaktionen. Über den Polen begünstigen diese Wolken aus Eiskörnchen Ozon abbauende Reaktionen, durch die die so genannten Löcher in der Ozonschicht entstehen – weshalb Millionen Menschen verstärkter ultravioletter Strahlung ausgesetzt sind. Chemische Reaktionen im Schnee am Boden können wiederum bodennahes Ozon und andere Umweltgifte produzieren. Organische Gifte und Quecksilber reichern sich im Schnee an und sickern über Flüsse und Ozeane in die Nahrungskette, wenn es taut.
Die molekularen Mechanismen, auf denen diese Prozesse basieren, sind bislang jedoch noch weit gehend unbekannt. Doch ohne genauere Kenntnisse, wie und wo chemische Reaktionen in Eis und Schnee ablaufen, kann man unmöglich Schnee- oder Eiswolkenmodule für Klimastudien entwickeln oder Laborergebnisse fundiert auf Freilandbedingungen übertragen. Fortschritte bei Computersimulationen und Analysemethoden – etwa oberflächensensitive Spektroskopie, die mittlerweile auch unter eisigen Temperatur- und Druckbedingungen funktioniert – ermöglichen nun jedoch neue Forschungsansätze.
Zehn ungeklärte Fragen
Wie formt sich Eis? Viele physikalische Details dazu, wann und wie Wasser gefriert, fehlen noch, obwohl das zum Verständnis unseres Klimas und des Wasserkreislaufs unabdingbar ist. Man kann bislang noch nicht mit Gewissheit vorhersagen, wo sich Eiswolken in der Atmosphäre bilden werden: Manche Himmelsabschnitte bleiben feucht, obwohl ihr Wasser wegen der äußeren Bedingungen gefrieren müsste. Vereisen Wassertropfen von innen nach außen oder kristallisieren sie vom Zentrum aus? Welche Art von Eis bildet sich dann? Eis entsteht dagegen oft leicht auf festen Oberflächen. Warum das geschieht, lässt sich nur herausfinden, wenn man die molekularen Grundlagen des Zusammenspiels zwischen den Wasserteilchen und der Oberflächen untersucht.
Wie verändert sich die Eisstruktur? Eiskristalle bestehen aus Wassermolekülen, die durch Wasserstoffbrückenbindungen regelmäßig tetraedrisch angeordnet sind. Viele kristalline Strukturen des Wassers sind bekannt – darunter die wohl gängigste, das hexagonale Erscheinungsbild der Kristalle in Schneeflocken. Da Druck und Temperatur schwanken, passt sich die Anordnung der Wassermoleküle entsprechend an, um stets im energetisch günstigsten Zustand vorzuliegen: Daraus entwickeln sich die verschiedenen Phasen des Eises. Die Phasenübergänge sind auf makroskopischer Ebene gut verstanden; nun müssen jedoch die zu Grunde liegenden molekularen Prozesse in Computersimulationen oder quantenchemischen Berechnungen reproduziert werden – und zwar über alle Temperatur- und Druckbereiche hinweg. Erst dann können wir Fragen zur Oberflächenstruktur beantworten oder wie sich Fremdkörper im Schnee auswirken.
Wie verhalten sich unterschiedliche Eisstrukturen? Zusätzlich zu geordneten Kristallstrukturen kann Eis auch in amorphen und metastabilen Ausprägungen vorliegen – molekulare Anordnungen, die zwar stabil sind, sich aber nicht im energetisch günstigsten Zustand arrangieren. Diese Vielfalt sorgt dafür, dass es viele Möglichkeiten gibt, wie schnell sich Eis bilden kann, wie reaktiv Eiswolken sind, wie Schmutz in Kometen eingeschlossen wird und welche mechanische Beanspruchung Eis im All aushält. Doch auch hier existieren noch viele Verständnislücken, wie dieses Eis strukturiert ist, ob es sich mit kristallinem Eis vermengt und wo es vorkommt. Amorphe Gefrornis – lose tetraedrisch in seinem Molekülaufbau, aber nicht durchgängig kristallin – bildet sich womöglich in Kometen, wenn Wasser bei extremen Minusgraden kondensiert. Metastabiles kubisches Eis wiederum, das sich einfacher an Kondensationskeime anlagert als hexagonale Formen, kann sich in Eiswolken entwickeln. Optisch sind beide Erscheinungsformen quasi nicht unterscheidbar, und man kommt nur sehr schwer an sie heran. Das macht ihre Erforschung kompliziert, doch Röntgenstrahlen und Neutronenbeugung im Labor könnten ihre Geheimnisse enthüllen.
Welche Oberflächenstrukturen kennzeichnen Eis? Die molekulare Ordnung bricht an der Kristalloberfläche zusammen. Nach außen gerichtete, freie Bindungsstellen an der Eisoberfläche binden neben weiteren Wassermolekülen auch Schadstoffe wie Methanol, Azeton, Salpeter- und Salzsäure, weshalb die resultierenden Wassermolekülnetzwerke unregelmäßig ausfallen und schwer zu beschreiben sind. Das gilt vor allem, wenn das Eis relativ warm ist und kurz vor seinem Schmelzpunkt steht. Dann breitet sich die Unordnung tief in die Kristalle hinein aus. Wesentliche Erkenntnisse zu dieser Schicht fehlen noch, etwa ihre Molekülstruktur und wie sich diese mit der Temperatur ändert. Außerdem ist noch ungeklärt, welche Rolle diese Grenzschicht bei der Einlagerung von Verschmutzungen spielt und wie sie chemische Reaktionen beeinflusst.
Wo kommen Unreinheiten im Eis vor? In der oberen Atmosphäre und im Weltraum ist Wassereis meist vermischt mit Kohlenmonoxid, Kohlendioxid, Methan, Schwefel- und Salpetersäure. Eis auf der Erdoberfläche beinhaltet Verbindungen aus den unterschiedlichsten Quellen wie Meersalz und Staub oder Schadstoffe aus Menschenhand. Wenn sich Kometen der Sonne nähern, verdampfen von ihrer Oberfläche ebenfalls Beimischungen, was andeutet, dass sie im gefrorenen Material eingeschlossen sind, bis dieses sich verflüchtigt. Noch hat die Forschung allerdings keine Ahnung, wie sich diese Verunreinigungen mit dem Eis mischen und ob unterschiedliche Eistypen wie weicher Schnee oder zusammengepresste Gletscher diese Fremdstoffe in ähnlicher Weise in sich behalten. Einige kristalline Strukturen, die mit Verschmutzungen zusammenhängen, konnten im Labor schon identifiziert werden: Salpetersäure beispielsweise bildet feste Hydrate mit gefrorenem Wasser, die eine kritische Rolle beim Ozonabbau in der Stratosphäre spielen. Wir müssen die Phasen, die Verteilung und den Chemismus der Unreinheiten innerhalb der Eismatrizen im All, in Wolken und auf dem Erdboden klären – etwa durch oberflächensensitive Spektroskopie.
Wie laufen Reaktionen im Eis ab? Am Südpol reichen die Reaktionen von aus dem Schnee ausgasenden Stickoxiden aus, um lokal die Konzentrationen an bodennahem Ozon so anzuheben, dass sie jenen von Industriegebieten gleichen. In der Arktis wandeln sich Quecksilberverbindungen aus der Atmosphäre im Schnee um, bevor sie wieder zurück in die Luft gelangen. Im Weltraum bilden sich Moleküle wie Wasserstoffgas, Wasser, Methanol, Kohlendioxid, Ammonium oder Aminosäuren sogar erst auf der Oberfläche von Eiskörnchen. Diese Entwicklungen vollziehen sich auf Wasserfilmen auf der Eisoberfläche und in komplexen Matrizen – um sie zu verstehen, müssen unter anderem die vorherrschenden Reaktionswege entschlüsselt werden.
Enthält das Eis Flüssigkeitsblasen? Sole füllt die Poren und Kanäle im Packeis; Meersalz und Unreinheiten an Körnchenrändern in Gletschern lösen lokales Schmelzen aus, die in Wasserblasen enden können. Diese Flüssigkeiten wiederum beeinflussen das Schicksal der Verschmutzungen selbst und die Stabilität des Eises. Noch ist aber unklar, wie viel flüssiges Wasser ein Gletscher speichern kann oder wo es sich darin befindet. Im Labor gefrieren Flüssigkeiten in winzigen, nur Nanometer großen Eistaschen bereits bei Temperaturen, die dutzende Grad Kelvin tiefer liegen als in der normalen Umwelt. Noch ist nicht bekannt, ob derartige Hohlräume auch in der Natur vorkommen und wie viel Schmutz sie in sich sammeln. Beobachtungen auf dieser Maßstabsebene sind schwierig; und flüssiges beziehungsweise gefrorenes Wasser lässt sich optisch kaum unterscheiden, doch könnten hier Chemikalien helfen, die den Kontrast zwischen beiden Phasen verstärken.
Wie beeinflussen physikalische Prozesse die Unreinheiten im Eis? Schnee absorbiert rasch Substanzen aus der Atmosphäre, die sich in Gletschern anschließend über die Jahrhunderte immer tiefer verlagern, was die chemische Zusammensetzung von Luft, Schnee und Eis im Lauf der Zeit verändert. Konzentrationsschwankungen von sich langsam verteilenden Schadstoffen wie Fluoriden und Methansulfonaten, verkomplizieren die zeitliche Bestimmung ihres Eintrags in den Eisbohrkernen. Welche Prozesse die Ausbreitung von Verschmutzungen in Eis und Schnee dominieren und wie der Austausch mit der Atmosphäre in Wolken oder am Boden abläuft, muss noch aufgeklärt werden. Adsorption an der Oberfläche, die Diffusion in die Eiskristalle oder an den Rändern der Eiskörnchen beeinflussen die Ausbreitung und die Fortentwicklung dieser Verbindungen ebenso wie Flüssigkeiten im Eis, in denen sie sich ansammeln.

Der Pine-Island-Gletscher gehört zu den schnellsten Gletschern der Antarktis: Er schiebt etwa 80 Kubikkilometer Eis jährlich ins Meer. Mit dem IceBridge-Programm wollen die Wissenschaftler umfassende Daten rund um das Verhalten des Gletschers sammeln, da sein Beitrag zu den steigenden Meeresspiegeln im Rahmen des Klimawandels bislang noch schwer einzuschätzen ist.
Zuletzt kalbte der Gletscher im Jahr 2001, und auch damals hatte sich im Vorjahr ein langer Riss gezeigt. Bisher stammten solche Aufnahmen allerdings von Satelliten, nun können die Forscher das Geschehen im Detail vom Flugzeug aus verfolgen.
Ein Video und weitere Bilder finden sich auf der Homepage des IceBridge-Projekts. Das oben gezeigte Bild stammt vom 26. Oktober 2011.
Wie beeinflusst das Eiswachstum die Kontaminationen? Wassermoleküle in den oberflächennahen Schichten von Eis und Schneeablagerungen verdunsten kontinuierlich in die Umgebung und frieren wieder an. Im Lauf eines Tages können so mit den wechselnden Temperaturen bis zu 60 Prozent der Moleküle umverteilt werden. Wie reagieren die eingelagerten Fremdstoffe, wenn sich die Form, die Oberfläche und das Volumen des Eises so drastisch ändern? Labor- und Geländearbeiten deuten an, dass Quecksilber, Wasserstoffperoxid, Salz- und Salpetersäure leichter von wachsenden denn von stabilen Eislagen aufgenommen werden. Experimentell gilt es herauszufinden, um welche Größenordnungen es sich dabei handelt.
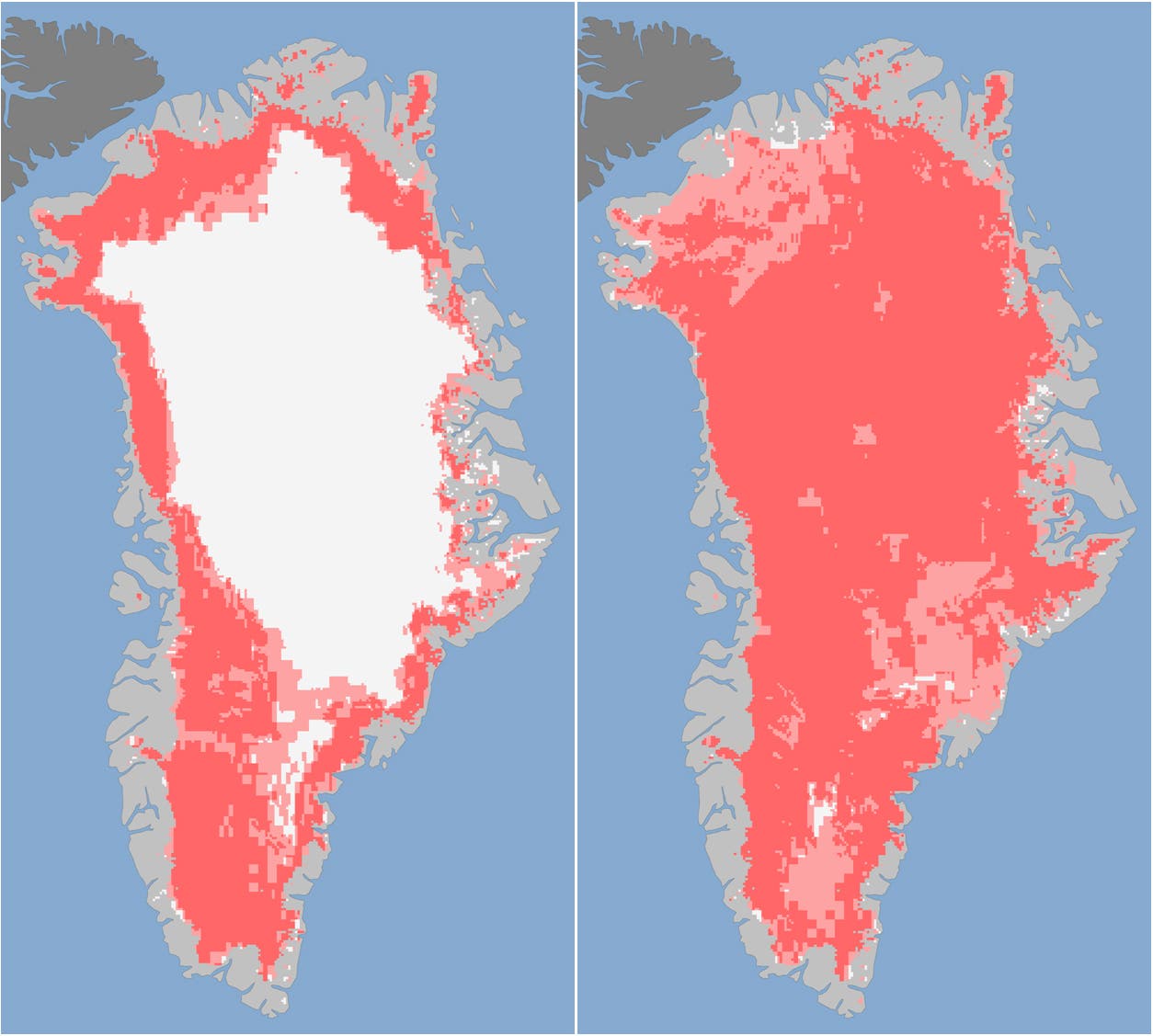
Wie lange überdauert das Eis noch? Satellitendaten belegen, dass gegenwärtig die Fläche von mehrjährigem Eis im Arktischen Ozean pro Jahrzehnt um zehn Prozent abnimmt. Die Gletscherschmelze auf Grönland und in der Antarktis beschleunigt sich. Aber noch verstehen wir nur ungenügend, wie schnell das Eis zukünftig bis zum Ende des Jahrhunderts schwindet. Bessere Vorhersagen lassen sich erzielen, wenn wir den Einfluss der Eischemie auf die molekulare Ebene der Schmelzprozesse erforschen.
Zurück ins Labor
Wie ließen sich diese zehn Fragen beantworten? Beginnen könnten wir mit den schon vorhandenen Forschungsnetzwerken wie dem Air-Ice Chemical Interactions Programme des International Global Atmospheric Chemistry Projects, den Arbeiten zur Mikrodynamik von Eis – genannt Micro-DICE – der European Science Foundation oder ArcRisk, das sich Gesundheitsrisiken in der Arktis widmet. Ihre Basis sollte aber erweitert werden: Benötigt werden unter anderem Materialwissenschaftler, die Kristall- und Oberflächenstrukturen von Metallen untersuchen, Zellbiologen, die sich der Lebenswelt gefrorener Ökosysteme annehmen, und Lebensmittelforscher, die beobachten, wie sich Inhaltsstoffe beim Gefrieren verändern.
Etwas mehr als fünf Millionen Euro könnten bereits ausreichen, um die offenen Punkte der Kryosphärenforschung zu bearbeiten. Und auch wenn es vielleicht schwerfällt, dieses Geld aufzutreiben, so ist nun doch die Zeit gekommen, die Erforschung der Eiswelten aus dem Gelände wieder etwas zurück ins Labor zu verlagern. Die Eischemie ist so wichtig, dass wir ihr endlich mit vielschichtigen, klar definierten Experimenten zu Leibe rücken müssen. Mit der Expertise, die wir in den letzten Jahrzehnten draußen bereits gewonnen haben, sollten wir dann endlich die Bedeutung von Eis und Schnee für den Planeten entschlüsseln – bevor beides verschwindet.





Schreiben Sie uns!
Beitrag schreiben