Tumormedizin: Ras ist wieder da
Als Stephen Fesik die Pharmaindustrie verließ, um an der Universität ein Labor zur Entwicklung neuer Medikamente einzurichten, machte er sich erst einmal eine Liste der fünf wichtigsten bekannten Krebsproteine. Für das Tumorwachstum sind sie essenziell – für das Drug-Discovery-Labor ein Albtraum: Sie sind einfach zu glatt, zu biegsam oder zu wählerisch, um Medikamente andocken und sich in ihrem Tun aufhalten zu lassen. Im Wissenschaftsjargon: Sie sind "undruggable", also "unmedikamentierbar".
Ganz oben auf Fesiks Liste stand die Familie der Ras-Proteine, deren Mitglieder seit mehr als 30 Jahren bekannt sind und deren mutierte Formen zu den wichtigsten Antreibern von Krebs zählen. Sie finden sich in den aggressivsten und tödlichsten Krebsarten, wie etwa einem Viertel aller Lungentumoren und 90 Prozent der Pankreaskarzinome. Bei manchen Arten fortgeschrittener Tumoren wurden ras-Mutationen auch mit früherem Versterben in Zusammenhang gebracht.
Doch machte sich die jahrzehntelange Forschung bisher in keinem einzigen Medikament bezahlt, das die Aktivität der Ras-Proteine sicher dämpfen könnte. Nach vielen Fehlschlägen in der Vergangenheit zogen sich daher die Pharmaunternehmen mehr und mehr aus entsprechenden Projekten zurück. Fesiks neues Labor an der Vanderbilt University in Nashville, Tennessee, und eine Hand voll anderer Teams wollen nun aber wieder daran arbeiten. Die inzwischen ausgefeilteren Technologien und das bessere Verständnis des Ras-Netzwerks kommen den Forschern dabei zugute. Letztes Jahr hat das US National Cancer Institute die so genannte Ras-Initiative gestartet, bei der mit jährlich zehn Millionen Dollar neue Wege zur Behandlung von Ras-abhängigen Tumoren gesucht werden sollen. Die Wissenschaftler sind schon dabei, Substanzen ausfindig zu machen, die – mit etwas Nachbesserung – irgendwann einmal die ersten Medikamente gegen Ras-Proteine werden könnten.
Den Forschern ist klar, dass noch viele Hürden zu überwinden sind. "Mit Ras ist nicht zu spaßen", weiß Troy Wilson, der Vorsitzende des Unternehmens Wellspring Biosciences, das im Jahr 2012 in La Jolla in Kalifornien gegründet wurde und auch auf Ras setzt. "Man darf es nicht unterschätzen, es ist eines der wichtigsten Onkogene."
Die Verfechter der Ras-Forschung wollen zudem auch aus kleinsten Fortschritten auf die anderen harten Brocken unter den Krebsproteinen übertragen lernen. Und nur weil viele das Ras-Protein als zu schwieriges Ziele sehen, dürfe die Wissenschaft noch lange nicht aufgeben, findet der Krebsforscher Channing Der von der University of North Carolina in Chapel Hill. "Auch Dogmen sind schließlich nicht unveränderlich."
Hochgesteckte Ziele
Schon 1982 konnte das Team um Der zeigen, wie Mutationen in ras-Genen Krebs auslösen. Das war der Höhepunkt einer Jagd nach Onkogenen – jenen Genen des Menschen, die Krebs vorantreiben. Anfangs kannte man sie nur aus Viren und Tiermodellen. Die Entdeckungen um Ras legten dann den Grundstein für den gigantischen Krebsforschungsapparat, der sich der Entschlüsselung genetischer Mutationen und dem Mapping veränderter molekularer Signalwege verschrieben hat. Gleichzeitig wuchs die Hoffnung auf neue Medikamente zur Heilung so mancher Krebsarten.
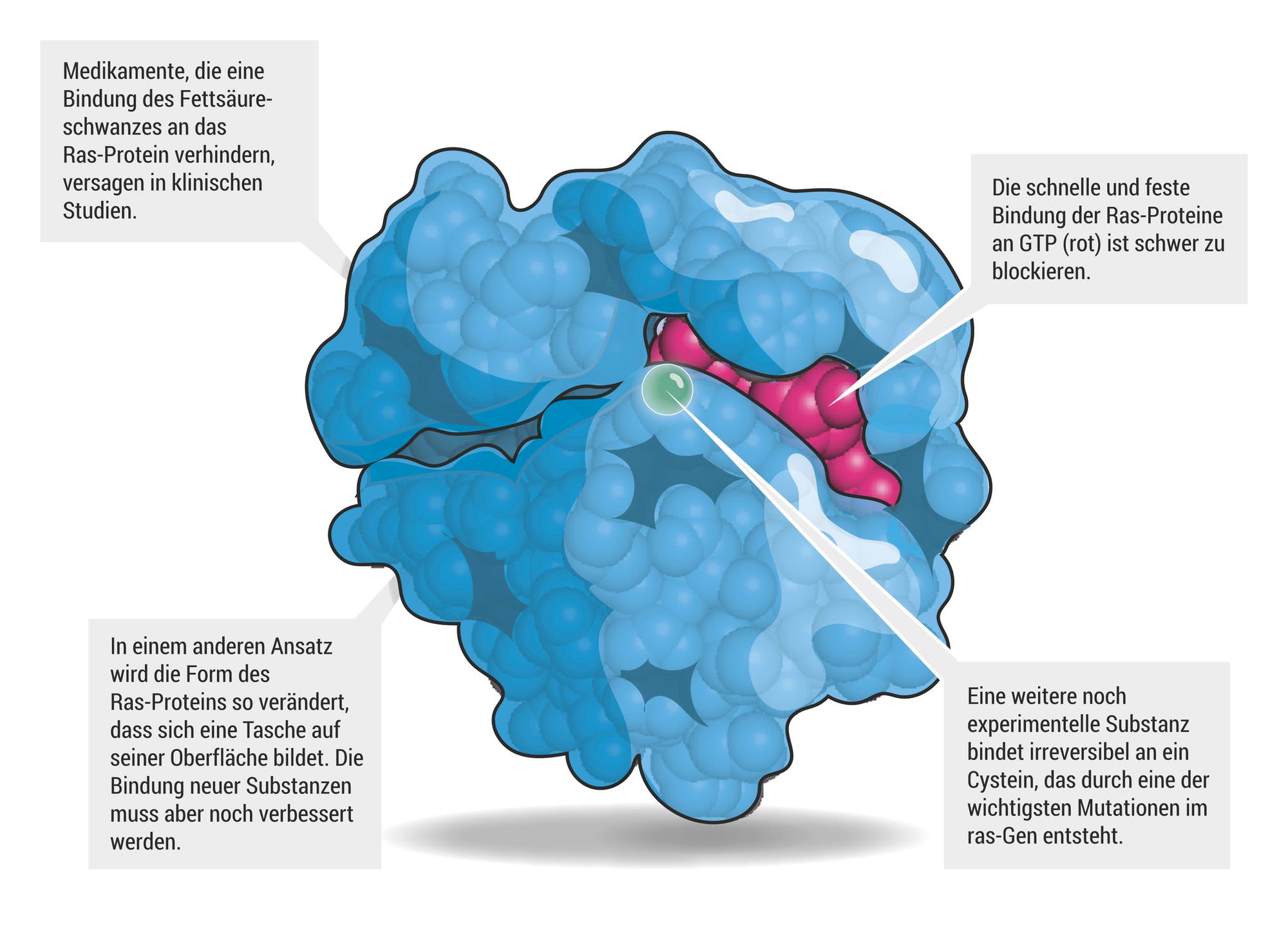
In den darauf folgenden Jahren jagte eine Beobachtung die andere. Dabei wurde klar, dass es im Menschen drei sehr ähnliche Ras-Proteine gibt, die bei der Zellproliferation, beispielsweise beim Ersatz von geschädigtem Gewebe, aktiviert werden. In normalen Zellen schalten Signale von außerhalb der Zelle das Ras-Protein ein, das anschließend an ein Molekül namens GTP bindet. Krebs auslösende Formen der Ras-Proteine können nicht mehr abgeschaltet werden, und daher schien es logisch, nach Medikamenten zu forschen, welche die GTP-Bindung von Ras stören und so das mutierte Ras in seiner Aktivität hemmen.
Aber je mehr über Ras bekannt wurde, desto pessimistischer schätzten die Forscher die Erreichbarkeit ihres Ziels ein. Es stellte sich nämlich heraus, dass die Ras-Familie eine extrem hohe Affinität für GTP hat, so dass es schier unmöglich schien, eine blockierende Substanz zu finden. Weil Ras in der Zelle mit anderen Proteinen interagiert, wären so genannte "small molecules" – niedermolekulare Substanzen, die in Zellen eindringen können – eine andere Möglichkeit. Doch diese sind meist zu klein, um die große Oberfläche abzudecken, die bei der Protein-Protein-Interaktion wie zwischen Ras und GTP beteiligt ist. Antikörper wären hier eigentlich gut geeignet, die meisten von ihnen können aber nicht einfach in Zellen hineingelangen.
Zusätzlich machte die Struktur des Ras-Proteins den Forschern zu schaffen. Bei der Medikamentenentwicklung wird anfangs anhand der Form eines Proteins abgeschätzt, mit welcher Wahrscheinlichkeit eine Substanz zu finden ist, die an eine bestimmte Stelle binden kann. Am besten für die Entwicklung eines Wirkstoffs sind Proteine mit tiefen Taschen, in die eine Substanz hineinschlüpfen und an verschiedenen Punkten anlegen kann – die Ras-Proteine haben jedoch eine relativ glatte Oberfläche.
Vor 20 Jahren dachten Forscher schon einmal, die Lösung des Problems gefunden zu haben. Damit Ras-Proteine funktionieren, müssen sie nämlich an der Innenseite der Zellmembran über einen Fettsäurerest einrasten. Dieser Schwanz wird vorab von einer Farnesyltransferase an Ras angeheftet – ein Enzym, das als Angriffspunkt für Medikamente besser geeignet wäre als die Ras-Proteine selbst. Ziel der Forscher war es nun, die Ras-Aktivität durch Hemmung der Farnesyltransferase zu inhibieren. Anfangs schien diese Strategie auch die ersehnte Lösung zu sein. Die Forscher fanden Farnesyltransferase-Inhibitoren, welche die Proliferation von Krebszellen aus der Maus wie auch dem Menschen blockierten, und Anfang des 21. Jahrhunderts wetteiferten mindesten sechs Pharmaunternehmen um ihre Markteinführung. Weil das Ras-Problem somit als gelöst schien, gaben sogar viele Wissenschaftler ihre eigenen Ansätze auf, erklärt der Chemiker Herbert Waldmann vom Max-Planck-Institut für molekulare Physiologie in Dortmund. "Alle warteten nur gespannt darauf, wie es weitergeht", erinnert er sich.
Das Warten endete mit einer der größten Enttäuschungen in der Geschichte der Pharmazie, als nämlich ein Medikament nach dem anderen in der klinischen Studie scheiterte.
Channing Der forschte damals weiter an Ras und konnte, wie auch andere, vieles über die Biologie der Krebsgene lernen. Die drei Ras-Moleküle unserer Zellen besitzen eine fast identische Struktur und Sequenz, so dass die Forscher auch von einer ähnlichen Funktion ausgingen. Die meisten Werkzeuge für ihre Untersuchungen – Zellkulturen, transgene Mäuse und Antikörper – wurden anhand von H-ras entwickelt, das besser als die zwei anderen Gene zu handhaben ist. "Wir alle, mich eingeschlossen, wollten uns mit den zwei anderen nicht herumschlagen, wo es doch noch vieles über H-ras zu lernen gab", erinnert sich Der. "Leider wurde hierbei eine ganze Menge Geld verbraucht."
In der Tat spielen nämlich die zwei anderen ras-Gene des Menschen, K-ras und N-ras, eine viel wichtigere Rolle bei der Entstehung von Krebs als das bis dahin am meisten untersuchte H-ras. Wie wir inzwischen wissen, besitzt die Zelle eine Art Notfallplan, um auch bei Störungen auf jeden Fall weiterarbeiten zu können. Wenn beispielsweise kein Farnesylrest vorhanden ist, können andere Enzyme das Ras-Protein an einen Fettsäurerest binden und auf diese Weise die Hemmsubstanzen ins Leere laufen lassen.
Diese Beobachtung traf das ganze Forschungsfeld schwer, und es dauerte einige Zeit, bevor überhaupt wieder einige bereit waren, hier weiter zu forschen. "Etwa ein Jahrzehnt später waren es dann auf einmal ganz viele, und Ras galt wieder als eines der wichtigsten Ziele in der Onkologie. Zehn Jahre lang hat sich hier nichts getan, packen wir es nun an, war die neue Devise", erinnert sich Waldmann. Dieses Mal verfolgten die Wissenschaftler aber einen ganz anderen Ansatz und schauten nach Schwachstellen in den Ras-getriebenen Tumoren.
Als eine dieser Schwächen gilt die so genannte synthetische Letalität. Wenn Ras-Proteine völlig übersteuert sind, werden oft andere molekulare Signalwege für das Überleben der Krebszellen wichtig, was viele Labors dazu brachte, nach synthetisch letalen Interaktionspartnern der mutierten ras-Gene zu suchen. Durch ihre Blockade sollten sich die Krebszellen umbringen lassen, während die normalen Zellen verschont blieben.
Das Ergebnis der Untersuchungen war eine Welle von Veröffentlichungen über mögliche neue Zielmoleküle, so genannte Targets – allerdings dicht gefolgt von einer nächsten Welle von Papern zur mangelnden Reproduzierbarkeit der Daten. Bei einer Konferenz im vergangenen Oktober berichtete dann William Sellers, der Leiter der Onkologie des Schweizer Pharmaherstellers Novartis, wie es ihnen nicht gelungen war, das prominenteste Paper zum Konzept der synthetischen Letalität zu reproduzieren. Alle Veränderungen im Labor, sei es der verwendete Zelltyp oder bestimmte Screening-Bedingungen, können das Ergebnis eines Experiments beeinflussen, weiß der Krebsforscher Julian Downward vom Francis Crick Institute in London. Viele seiner Kollegen durchkämmen nach wie vor die bekannten Datensätze auf der Suche nach geeigneten Zielmolekülen, aber Downward zweifelt an ihrem Erfolg. "Jeder hat irgendwie andere Ergebnisse", sagt er, "und ich fürchte, das sind alles nicht die erfolgreichsten Ziele."
Passgenau
Nach den Enttäuschungen bei der Suche nach synthetisch letalen Interaktionen versuchten es einige Wissenschaftler mit direkter Blockade. "Wir wollten nun Ras direkt angehen", sagt der Biochemiker Brent Stockwell von der Columbia University in New York. Die Fortschritte der letzten fünf Jahre im Bereich Computermodelling und Screening nach therapeutisch einsetzbaren Substanzen lässt alle hoffen, doch noch Möglichkeiten zur Attacke auf Ras zu finden, trotz seiner glatten Oberfläche ohne Taschen zum Hineinschlüpfen, sagt Stockwell. Inzwischen lässt sich ja auch die Affinität von "small molecules" genauer vorhersagen, und die Dynamik der Proteine wird besser verstanden.
Stockwells Team baut ebenfalls darauf und will zuerst am Computer und später im Labor "small molecules" entwickeln, die genau zur Oberfläche von Ras passen. "Vielleicht gibt es ja da draußen in der Natur einfach nichts Passendes, und wir müssen die Inhibitoren synthetisch herstellen", erklärt er. Auch Fesik baut an neuen Medikamenten, geht aber von einer Datenbank bekannter Substanzen aus. Bisher arbeitete er bei Abbott Laboratories in Abbott Park in Illinois an Möglichkeiten, die Protein-Interaktionen zu zerstören. Hierzu setzte er Fragmente von immerhin schwach an ihr Ziel bindenden Substanzen zu neuen großen Substanzen zusammen, die es als solche in den Datenbanken des Drug Design nicht gibt.
Fesik vergleicht die Technik dieses Fragment-based-Screenings in etwa mit der Anfertigung eines Schlüssels für ein ganz bestimmtes Schloss. Man baut nach und nach verschiedene Stückchen mit Kerben und "kombiniert diese schließlich", erklärt er. "Die erhaltenen Substanzen wurden nie zuvor hergestellt und werden hier vollkommen neu und Schritt für Schritt an das gewünschte Protein angepasst."
Fesiks Labor und seine Kooperationspartner in der Industrie fanden auf diese Weise mehr als 130 Moleküle, die zumindest schwach an K-Ras binden und die Proteinstruktur dabei so verändern, dass eine Tasche in der Moleküloberfläche entsteht. Nun wollen die Forscher noch weitere Fragmente anfügen, um die Passgenauigkeit zu verbessern, sozusagen die zweite Kerbe im Schlüssel. Channing Der weiß, dass sich Fesik schon vor seiner akademischen Karriere in der Industrie einen Namen gemacht hat auf der Suche nach Substanzen gegen "undruggable" Targets. "Wenn es überhaupt jemand schafft, dann Fesik", sagt er.
Andere Forscher wollen eher spezifische Mutationen im K-ras-Gen ausnutzen. Zwar sind viele verschiedene mit Krebs assoziierte Mutationen bekannt, doch nur drei davon spielen bei den Ras-getriebenen Tumoren eine Rolle. Jede der Mutationen führt zu einem Enzym mit leicht verändertem Verhalten, erklärt Channing Der. "Wenn wir jede Mutation als individuelle Veränderung ansehen, ergeben sich bisher einmalige Angriffsmöglichkeiten."
Der Biochemiker Kevan Shokat von der University of California in San Francisco arbeitet seit sechs Jahren auf diesem Gebiet. Im Jahr 2013 präsentierte er eine Substanz gegen die Mutation G12C im K-ras-Gen. Sie findet sich bei 20 Prozent aller Fälle von Lungenkrebs und führt zum Austausch der Aminosäure Glycin gegen Cystein, was dann das entstandene Protein mit anderen reagieren lässt. Shokats Substanz nützt ebendieses reaktive Cystein aus und bindet hierüber irreversibel an das mutierte K-Ras. Der Inhibitor bedarf zwar noch etwas Veränderung, bevor er beim Patienten eingesetzt werden kann, er ist aber der erste Kandidat zur direkten Attacke gegen Ras. Der neue Ansatz hat natürlich für enorme Aufregung gesorgt und "das ganze Feld wieder zum Leben erweckt", erzählt Downward.
Shokat hat schon lange von einem mutationsspezifischen Ansatz geträumt, aber bisher immer gezögert, diesen im Labor tatsächlich anzugehen. Substanzen, die schnell, fest und kaum wieder ablösbar am Zielmolekül binden, könnten vielleicht auch zum Problem werden: Es drohen unvorhersehbare Reaktionen mit anderen Proteinen im Körper; Nebenwirkungen sind also nicht auszuschließen. Allerdings: Auch einige bereits erfolgreiche Medikamente, wie Ibrutinib gegen Lymphome und Myelome, binden irreversibel an ihr Zielmolekül.
"Zehn Jahre lang hat sich hier nichts getan – packen wir es nun an!"
Inzwischen interessieren sich immer mehr Pharmakonzerne für Medikamente, die nur in Patienten mit bestimmten Mutationen wirken. "Es gibt sicherlich nicht ein einziges Medikament für alle Patienten mit K-Ras-abhängigen Tumoren", meint der Krebsforscher Timothy Burns von der University of Pittsburgh in Pennsylvania.
Wie auch immer die Lösung des Puzzles um Ras aussehen wird, Fesik ist sich sicher, dass sie aus einer universitären Einrichtung kommt. Er wollte immer an Hauptschaltern der Zelle arbeiten, egal ob sie einfache oder schwierige Zielmoleküle sind, und hat deshalb die Pharmaindustrie verlassen. In Firmen ist die Jagd nach einem als "undruggable" verschrienen Protein schwer zu rechtfertigen, weil hier wissenschaftliches Interesse oftmals hinter möglichst rasch erfolgversprechenden Ansätzen zurückstehen muss. "Die meisten Unternehmen wollen das Risiko nicht eingehen, und wenn sie es wagen, dann nur für kurze Zeit", kommentiert er seine Entscheidung, den Arbeitsplatz zu wechseln.
Doch es werden schon Brücken gebaut zwischen Universität und Industrie. So hat sich Fesiks Labor zum Testen seiner ersten Generation der Ras-bindenden Substanzen mit der Pharmafirma Boehringer Ingelheim zusammengetan, und Shokat ist Mitbegründer der Firma Wellstring Bioscienes, die inzwischen gemeinsam mit Janssen Biotech aus Horsham in Pennsylvania seinen neuen Inhibitor auf den Markt bringen will.
Auch die staatlichen Stellen werden langsam hellhörig und fördern mit der multimillionenschweren Ras-Initiative die Forschung an Methoden und Grundlagen zur Proteinstruktur des Onkogens, um so die Medikamentenentwicklung zu unterstützen, erklärt Frank McCormick von der University of California in San Francisco und Koleiter des Projekts. "Wir wollen das Risiko in der Ras-Forschung verringern und so andere Wissenschaftler wieder mit ins Boot holen."
Viele Jahre lang hat die Pharmaindustrie laut McCormick bei den Kinasen richtiggehend abgesahnt. Das sind einfachere Ziele, und viele nützliche Medikamente wurden schon entwickelt. Doch die Welle ebbt langsam ab, und es ist seiner Meinung nach an der Zeit, nach Höherem zu greifen und sich mit schwierigeren, für die Zelle aber essenziellen Zielmolekülen zu beschäftigen. Stockwell hofft, dass sich das aktuelle Rennen um die Ras-Proteine auch auf andere harte Brocken überträgt. "Wenn die Arbeiten Erfolg haben, wird die Begeisterung auch die Jagd auf andere Zielproteine beflügeln", glaubt er. "Wir haben noch viel Spielraum, um mit bisher unangetasteten Zielmolekülen gegen Krebs vorzugehen."
Der Artikel ist als "Cancer: The Ras renaissance" in "Nature" erschienen.



Schreiben Sie uns!
Beitrag schreiben