News: Warum Stahl durch den Rost fällt
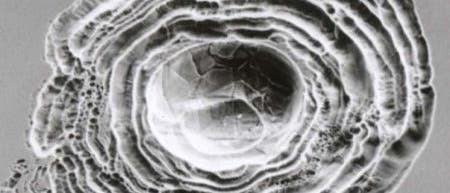
So auch Mary Ryan vom Imperial College of Science, Technology and Medicine und David Williams vom University College London. Sie untersuchten rostfreien Stahl mithilfe eines speziellen Mikroskops, welches einen fokussierten Ionenstrahl (FIB) auf die Probe wirft.
Dabei handelt es sich um energiereiche geladene Teilchen (Ionen), die im Unterschied zu Photonen nicht reflektiert werden, sondern Partikeln aus der Oberfläche ihre eigene Ladung übertragen und sie in Gegenrichtung beschleunigen. Schließlich landen die ionisierten Teilchen in einem Massenspektrometer. Auf diese Weise erhalten die Forscher quasi eine chemische Landkarte der Probenoberfläche.
Diese Oberflächenschicht enthält neben Eisen auch Chromoxide - entstanden aus dem Legierungsbestandteil Chrom und Luftsauerstoff. Wie eine Haut schützt diese Verbindung das darunter liegende Metall vor Korrosion. Und selbst wenn diese Haut Kratzer bekommt - sie "heilt" wieder, weil Chrom gleichmäßig im Stahl verteilt ist, bei Bedarf oxidiert und somit Chromoxid nachbildet.
Nun zeigte das chemische Abbild allerdings Bereiche, in denen Chromoxid fehlt. Als Ursache machten die Forscher kleine Einschlüsse von Schwefel aus, der als Verunreinigung des Eisens in den Stahl gelangt. Als Einschlüsse mit wenigen Mikrometern Durchmesser sind sie gefährliche Keimzellen für Löcher.
Die Schwefelklümpchen entstehen beim Abkühlen der Schmelze. Da der Schmelzpunkt des Schwefels unter dem des Eisens liegt, bleibt er auch dann flüssig, wenn das Eisen bereits erstarrt. So bilden sich Schwefeltröpfchen, die in der Lage sind, ihrer Umgebung das Chrom zu entziehen und zu binden. Bei weiter sinkender Temperatur erstarren sie zu kleinen Einschlüssen.
Überall dort, wo sich diese Fremdstoffe sammeln, verarmt der Stahl also an Chrom. Schwerwiegende Folgen hat dies an der Oberfläche, wo die Haut bei Wind und Wetter ihre schützende Wirkung verliert.
Zur Lösung des Problems schlagen die Forscher eine Hitzebehandlung vor, die dazu führt, dass Chrom wieder an jene Regionen diffundieren kann, denen es zuvor vom Schwefel entzogen wurde.

Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.