Stammzellforschung: Woher nehmen und nicht Leben stehlen?
Das heißeste Eisen der Medizin wird in der Stammzellforschung geschmiedet – wobei die Forscher ständig auf dem schmalen Grat zwischen Risiken und Chancen der Technik und in einem gesetzlichen Grenzbereich voller ungelöster ethischer Probleme wandeln. Offensichtlich können neu entdeckte Möglichkeiten dabei gleichzeitig verkomplizieren und Auswege schaffen.
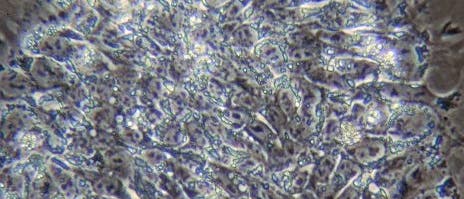
© Jeff Miller/University of Wisconsin-Madison (Ausschnitt)
Es scheint, als ob die Stammzellforscher nach dem Fälschungsskandal der Vergangenheit erst einmal Luft holen mussten – nun aber ist die Zeit des nur stillen Weiterforschens offenbar wieder vorbei. In einer Flut von Veröffentlichungen präsentieren zeitgleich mehrere Forschergruppen Beiträge, mit denen sie technische, medizinische und ethische Probleme ihres Forschungsfeldes überwinden wollen.
Genug solcher Schwierigkeiten türmen sich noch zwischen der optimistischen Heilserwartungen einer rosigen Zukunft mit angewandter, maßgeschneiderter Stammzelltherapie und der recht tristen Gegenwart des tatsächlich Machbaren. Besonders ein ethischer Knackpunkt zwingt die Forschergemeinde früh zur Richtungsentscheidung an einer Wegscheide: die Frage nach dem Woher des biologischen Rohstoffs, auf dessen Grundlage Menschen einmal geholfen werden soll. Dieser Rohstoff ist – beim einfachsten, derzeit viel versprechendsten, aber eben moralisch umstrittenen Ansatz – selbst ein Stück potenziellen Lebens: zum Beispiel eine Eizelle oder ein Embryo, aus dem ein Mensch werden könnte.
Die faszinierende Pluripotenz embryonaler Stammzellen soll die Grundlage sein bei der Entwicklung des therapeutischen Klonens, bei dem das Erbgut der Stammzelle durch das eines Patienten ersetzt wird. So geklonte Zellen und Gewebe, genetisch völlig identisch mit dem ihrer Erbgutspender, könnten dann einst etwa zu Ersatz-Organen herangezüchtet werden, die vom Körper nach einer Transplantation nicht als fremd erkannt und somit nie abgestoßen werden – ein Fernziel vorerst. Aber gerade dann, wenn diese Vision der Medizin tatsächlich wahr oder gar Routine geworden sein wird, stellt sich das Problem der Gewinnung der am Anfang verbrauchten Embryonen umso häufiger und dringlicher.
Eine ungelöste Frage der Ethik
Einige Forschergruppen beschreiten daher einen recht dornigen Umweg, auf dem moralische Bedenken nicht im Wege stehen: Sie wollen als Therapiewaffen vom Körper des Patienten selbst produzierte, adulte Stammzellen gewinnen, die sich auch bei Erwachsenen etwa im Knochenmark finden. Vermieden würde auf diesem Weg der gesellschaftspolitisch umstrittene Verbrauch von Embryonen. Einige Studien haben darauf hingedeutet, dass adulte Stammzellen, die aus einem Gewebetyp entnommen werden – zum Beispiel dem Blut – in einem anderen Gewebetyp neue Zelltypen bilden können – zum Beispiel Nervenzellen.
Der Weg zur notwendigen völligen Reprogrammierung zum unbeschriebenen Blatt ist allerdings weitaus dorniger, wenn die Wissenschaftler nicht von embryonalen, sondern von ausgereiften Zellen ausgehen. Nun aber glauben Wissenschaftler, entscheidend mehr über die biologischen Mechanismen dieses Umbaus zu universal einsetzbaren Stammzellen verstanden zu haben. Die Gruppen arbeiteten mit Fibroblasten, einer wenig spezialisierten Zellsorte des Bindegewebes, und ergänzen mit ihren Ergebnissen nun Resultate, die eine japanische Forschergruppe um Shinya Yamanaka von der Universität Kyoto schon im vergangenen Jahr vorgestellt hatte [1] und nun ausweitet [2].
Die japanischen Forscher hatten den Fibroblasten mit Hilfe von Viren-Fähren aktive Gene beschert, die normalerweise nur in embryonalen Stammzellen abgelesen werden. Die veränderten Zellen produzierten daraufhin die vier Transkriptionsfaktoren Oct3/4, Sox2, c-Myc und Klf4, deren Aktivität ausreichte, um die Zellen in einen pluripotenten Embryonalzustand zurückzuversetzen: Es entstanden "induzierte embryonale Stammzellen". Ein großer Schritt vorwärts – mit allerdings noch einigen Haken. So bestanden etwa Zweifel, ob sich die Zellen nicht etwa in bestimmter Hinsicht doch von embryonalen Stammzellen unterscheiden. Es gelang den Japanern zum Beispiel zunächst nicht, mit ihren Zellen tatsächlich lebende Mäuse heranzuziehen.
Nun vermeldete das japanische Team Erfolg. Den gleichen Schritt vollzogen zudem auch Rudolf Jaenisch vom Whitehead Institute for Biomedical Research und seine Kollegen, indem sie induzierte Stammzellen in Blastozysten injizierten und dabei lebensfähige Mäuse erhielten, in deren Keimdrüsen sich das geklonte Erbgut wiederfand [3]. Zudem konnten die Forscher mit einer Reihe von technisch ausgefeilteren Versuchen zeigen, wie ähnlich die Eigenschaften "induzierter" und "echter" embryonaler Stammzellen tatsächlich sind: Ob im DNA-Methylierungsmuster, der Genexpressionsrate oder dem Zustand des verpackten Erbguts als Chromatin, nirgendwo erkannten Jaenisch und Co augenfällige Unterschiede.
"Alle diese Ergebnis haben einen vorläufigen Charakter", meint Jaenisch – und ob sie im Menschen funktionieren, sei noch lange nicht geklärt. Immerhin aber ist nun prinzipiell der Beweis erbracht, dass der neuprogrammierte Zelltyp "alles kann, was traditionelle embryonale Stammzellen auch können". Vielleicht weisen die induzierten embryonalen Stammzellen aus adulten Zellen den Weg aus dem ethischen Dilemma der verbrauchenden Embryonenforschung. Jaenischs Teammitglied Marius Wernig teilt diese Hoffnung, warnt aber gleichzeitig davor zu glauben, man bräuchte schon jetzt keine Eizellen mehr zur Gewinnung embryonaler Stammzellen: "Dies zu behaupten, wäre voreilig und fahrlässig."
Fragwürdige Resteverwertung?
Tatsächlich beurteilen die Forscher die Möglichkeiten zurückhaltend, ihre Methode schon bald auch in menschlichen Zellen zu beherrschen. Und so bekommen ebenfalls jetzt veröffentlichte Ergebnisse eines Stammzell-Forscherteams eine größere Relevanz, das einen ganz anderen Ansatz verfolgt. Kevin Eggan, auch er vom Stem Cell Institute der Harvard-Universität, hat dabei mit seinen Kollegen an traditionellen embryonalen Stammzellen geforscht, gezielt Mäuseembryonen zum Zweck des therapeutischen Klonens erzeugt – und vor allem einen Weg vorgestellt, der gänzlich auf den sonst üblichen, ethisch fragwürdigen Verbrauch von entwicklungsfähigen Eizellen verzichtet [5].
Eggan und Co zeigten nun mit Mauszellen, dass sich statt unbefruchteter auch befruchtete Eizellen als Empfänger anbieten. Dazu mussten die Wissenschaftler nur die Zellteilung sowohl bei der Empfänger- als auch bei der Spenderzelle in einem bestimmten Stadium der Mitose durch einen Wirkstoff einfrieren. So wird nach dem Transfer der Spender-DNA dann offenbar ein totaler Neustart der Teilungen ermöglicht, wie die Wissenschaftler glauben – jedenfalls entwickelten sich mit der modifizierten Methode tatsächlich einige wenige lebende Klone bis zur Geburt, wobei die Tiere dann aber recht bald starben. Immerhin – aus so erzeugten Klonembryonen ließen sich embryonale Stammzellen gewinnen.
Die Ankündigung, ethische Probleme des therapeutischen Klonens so umgehen zu können, erscheint allerdings auf den ersten Blick zumindest fragwürdig. Eggan und Co haben zwar tatsächlich keine frischen unbefruchteten Eizellen für ihren Versuch gebraucht – dafür aber eben befruchtete. Hierbei könnte also vielleicht noch eher potenzielles Leben verhindert worden sein – was also insgesamt eher nach ethischem Rück- denn Fortschritt klingt, wenn man zudem bedenkt, dass die Erfolgsrate in keiner Weise über jener der etablierten Klonmethodik liegt.
Trotzdem sind Kommentatoren wie Alan Colman vom ES-Cell-International-Forschungsinstitut in Singapur beeindruckt [6]. Sie weisen auf ein Experiment von Eggans Team hin, bei dem nicht entwicklungsfähige befruchtete Mäuseeizellen mit einem dreifachen Chromosomensatz erfolgreich als Empfängerzellen benutzt wurden – nach dem Entkernen, der Injektion der Spender-DNA und dem Aufheben der Teilungsblockade entwickelten sich auch daraus einige Klone. Tatsächlich aber existiert eine recht große Zahl solcher potenzieller Empfängeroozyten mit vielfachem Chromosomensatz auch vom Menschen – sie fallen relativ oft, etwa in drei bis fünf Prozent aller Fälle, bei In-vitro-Fertilisationsversuchen an.
In den Kliniken werden solche befruchtete Eizellen mit mehr als doppeltem Chromosomensatz nicht implantiert, sondern aussortiert und vernichtet, denn aus ihnen könnten keine lebensfähigen Embryonen entstehen. Mit Hilfe von Eggans Methode wäre es aber denkbar, sie zu verwenden, um neue embryonale Stammzelllinien zu gewinnen – ganz ohne den fragwürdigen Entscheid, ein potenzielles Leben zu zerstören, kommentiert Colman. Weiter frische unbefruchtete Eizellen zu gewinnen und zu verbrauchen, wäre diesem Ansatz tatsächlich kaum vorzuziehen.
Genug solcher Schwierigkeiten türmen sich noch zwischen der optimistischen Heilserwartungen einer rosigen Zukunft mit angewandter, maßgeschneiderter Stammzelltherapie und der recht tristen Gegenwart des tatsächlich Machbaren. Besonders ein ethischer Knackpunkt zwingt die Forschergemeinde früh zur Richtungsentscheidung an einer Wegscheide: die Frage nach dem Woher des biologischen Rohstoffs, auf dessen Grundlage Menschen einmal geholfen werden soll. Dieser Rohstoff ist – beim einfachsten, derzeit viel versprechendsten, aber eben moralisch umstrittenen Ansatz – selbst ein Stück potenziellen Lebens: zum Beispiel eine Eizelle oder ein Embryo, aus dem ein Mensch werden könnte.
Die faszinierende Pluripotenz embryonaler Stammzellen soll die Grundlage sein bei der Entwicklung des therapeutischen Klonens, bei dem das Erbgut der Stammzelle durch das eines Patienten ersetzt wird. So geklonte Zellen und Gewebe, genetisch völlig identisch mit dem ihrer Erbgutspender, könnten dann einst etwa zu Ersatz-Organen herangezüchtet werden, die vom Körper nach einer Transplantation nicht als fremd erkannt und somit nie abgestoßen werden – ein Fernziel vorerst. Aber gerade dann, wenn diese Vision der Medizin tatsächlich wahr oder gar Routine geworden sein wird, stellt sich das Problem der Gewinnung der am Anfang verbrauchten Embryonen umso häufiger und dringlicher.
Eine ungelöste Frage der Ethik
Einige Forschergruppen beschreiten daher einen recht dornigen Umweg, auf dem moralische Bedenken nicht im Wege stehen: Sie wollen als Therapiewaffen vom Körper des Patienten selbst produzierte, adulte Stammzellen gewinnen, die sich auch bei Erwachsenen etwa im Knochenmark finden. Vermieden würde auf diesem Weg der gesellschaftspolitisch umstrittene Verbrauch von Embryonen. Einige Studien haben darauf hingedeutet, dass adulte Stammzellen, die aus einem Gewebetyp entnommen werden – zum Beispiel dem Blut – in einem anderen Gewebetyp neue Zelltypen bilden können – zum Beispiel Nervenzellen.
Der Weg zur notwendigen völligen Reprogrammierung zum unbeschriebenen Blatt ist allerdings weitaus dorniger, wenn die Wissenschaftler nicht von embryonalen, sondern von ausgereiften Zellen ausgehen. Nun aber glauben Wissenschaftler, entscheidend mehr über die biologischen Mechanismen dieses Umbaus zu universal einsetzbaren Stammzellen verstanden zu haben. Die Gruppen arbeiteten mit Fibroblasten, einer wenig spezialisierten Zellsorte des Bindegewebes, und ergänzen mit ihren Ergebnissen nun Resultate, die eine japanische Forschergruppe um Shinya Yamanaka von der Universität Kyoto schon im vergangenen Jahr vorgestellt hatte [1] und nun ausweitet [2].
Die japanischen Forscher hatten den Fibroblasten mit Hilfe von Viren-Fähren aktive Gene beschert, die normalerweise nur in embryonalen Stammzellen abgelesen werden. Die veränderten Zellen produzierten daraufhin die vier Transkriptionsfaktoren Oct3/4, Sox2, c-Myc und Klf4, deren Aktivität ausreichte, um die Zellen in einen pluripotenten Embryonalzustand zurückzuversetzen: Es entstanden "induzierte embryonale Stammzellen". Ein großer Schritt vorwärts – mit allerdings noch einigen Haken. So bestanden etwa Zweifel, ob sich die Zellen nicht etwa in bestimmter Hinsicht doch von embryonalen Stammzellen unterscheiden. Es gelang den Japanern zum Beispiel zunächst nicht, mit ihren Zellen tatsächlich lebende Mäuse heranzuziehen.
Nun vermeldete das japanische Team Erfolg. Den gleichen Schritt vollzogen zudem auch Rudolf Jaenisch vom Whitehead Institute for Biomedical Research und seine Kollegen, indem sie induzierte Stammzellen in Blastozysten injizierten und dabei lebensfähige Mäuse erhielten, in deren Keimdrüsen sich das geklonte Erbgut wiederfand [3]. Zudem konnten die Forscher mit einer Reihe von technisch ausgefeilteren Versuchen zeigen, wie ähnlich die Eigenschaften "induzierter" und "echter" embryonaler Stammzellen tatsächlich sind: Ob im DNA-Methylierungsmuster, der Genexpressionsrate oder dem Zustand des verpackten Erbguts als Chromatin, nirgendwo erkannten Jaenisch und Co augenfällige Unterschiede.
"Die Zellen leisten alles, was auch embryonale Stammzellen können"
(Rudolf Jaenisch)
Zu ähnlichen Ergebnissen kamen auch Konrad Hochedlinger vom Harvard Stem Cell Institute und sein Team, dem Jaenisch unter anderem ebenfalls angehörte [4]. Die Gruppe hatte sich insbesondere darauf konzentriert, den Prozess der Fibroblasten-Auswahl zu perfektionieren. Auch ihre Resultate legen nahe, dass sich die anfangs undifferenzierten Gewebezellen mit Hilfe der vier Transkriptionsfaktoren am Ende in pluripotente embryonalen Stammzellen gleichwertige Zellen zurückverwandeln – wobei zum Beispiel das eine inaktivierte von zwei X-Chromosomen in den Zellen erwachsener Mausweibchen wieder reaktiviert wird. (Rudolf Jaenisch)
"Alle diese Ergebnis haben einen vorläufigen Charakter", meint Jaenisch – und ob sie im Menschen funktionieren, sei noch lange nicht geklärt. Immerhin aber ist nun prinzipiell der Beweis erbracht, dass der neuprogrammierte Zelltyp "alles kann, was traditionelle embryonale Stammzellen auch können". Vielleicht weisen die induzierten embryonalen Stammzellen aus adulten Zellen den Weg aus dem ethischen Dilemma der verbrauchenden Embryonenforschung. Jaenischs Teammitglied Marius Wernig teilt diese Hoffnung, warnt aber gleichzeitig davor zu glauben, man bräuchte schon jetzt keine Eizellen mehr zur Gewinnung embryonaler Stammzellen: "Dies zu behaupten, wäre voreilig und fahrlässig."
Fragwürdige Resteverwertung?
Tatsächlich beurteilen die Forscher die Möglichkeiten zurückhaltend, ihre Methode schon bald auch in menschlichen Zellen zu beherrschen. Und so bekommen ebenfalls jetzt veröffentlichte Ergebnisse eines Stammzell-Forscherteams eine größere Relevanz, das einen ganz anderen Ansatz verfolgt. Kevin Eggan, auch er vom Stem Cell Institute der Harvard-Universität, hat dabei mit seinen Kollegen an traditionellen embryonalen Stammzellen geforscht, gezielt Mäuseembryonen zum Zweck des therapeutischen Klonens erzeugt – und vor allem einen Weg vorgestellt, der gänzlich auf den sonst üblichen, ethisch fragwürdigen Verbrauch von entwicklungsfähigen Eizellen verzichtet [5].
"Es wäre voreilig und unverantwortlich zu behaupten, wir könnten schon auf embryonale Stammzellgewinnung verzichten"
(Marius Wernig)
Klonorganismen – oder nur therapeutisch potenziell relevantes Klongewebe – entstehen derzeit, indem ihr Erbgut entfernt, durch das einer Spenderzelle ersetzt und eine Befruchtung durch chemische oder elektrische Reize suggeriert wird, worauf die ersten Zellteilungen einsetzen. Dabei lauern eine Reihe von Problemen – besonders, wenn menschliche Eizellen oder die von Primaten benutzt werden. (Marius Wernig)
Eggan und Co zeigten nun mit Mauszellen, dass sich statt unbefruchteter auch befruchtete Eizellen als Empfänger anbieten. Dazu mussten die Wissenschaftler nur die Zellteilung sowohl bei der Empfänger- als auch bei der Spenderzelle in einem bestimmten Stadium der Mitose durch einen Wirkstoff einfrieren. So wird nach dem Transfer der Spender-DNA dann offenbar ein totaler Neustart der Teilungen ermöglicht, wie die Wissenschaftler glauben – jedenfalls entwickelten sich mit der modifizierten Methode tatsächlich einige wenige lebende Klone bis zur Geburt, wobei die Tiere dann aber recht bald starben. Immerhin – aus so erzeugten Klonembryonen ließen sich embryonale Stammzellen gewinnen.
Die Ankündigung, ethische Probleme des therapeutischen Klonens so umgehen zu können, erscheint allerdings auf den ersten Blick zumindest fragwürdig. Eggan und Co haben zwar tatsächlich keine frischen unbefruchteten Eizellen für ihren Versuch gebraucht – dafür aber eben befruchtete. Hierbei könnte also vielleicht noch eher potenzielles Leben verhindert worden sein – was also insgesamt eher nach ethischem Rück- denn Fortschritt klingt, wenn man zudem bedenkt, dass die Erfolgsrate in keiner Weise über jener der etablierten Klonmethodik liegt.
Trotzdem sind Kommentatoren wie Alan Colman vom ES-Cell-International-Forschungsinstitut in Singapur beeindruckt [6]. Sie weisen auf ein Experiment von Eggans Team hin, bei dem nicht entwicklungsfähige befruchtete Mäuseeizellen mit einem dreifachen Chromosomensatz erfolgreich als Empfängerzellen benutzt wurden – nach dem Entkernen, der Injektion der Spender-DNA und dem Aufheben der Teilungsblockade entwickelten sich auch daraus einige Klone. Tatsächlich aber existiert eine recht große Zahl solcher potenzieller Empfängeroozyten mit vielfachem Chromosomensatz auch vom Menschen – sie fallen relativ oft, etwa in drei bis fünf Prozent aller Fälle, bei In-vitro-Fertilisationsversuchen an.
In den Kliniken werden solche befruchtete Eizellen mit mehr als doppeltem Chromosomensatz nicht implantiert, sondern aussortiert und vernichtet, denn aus ihnen könnten keine lebensfähigen Embryonen entstehen. Mit Hilfe von Eggans Methode wäre es aber denkbar, sie zu verwenden, um neue embryonale Stammzelllinien zu gewinnen – ganz ohne den fragwürdigen Entscheid, ein potenzielles Leben zu zerstören, kommentiert Colman. Weiter frische unbefruchtete Eizellen zu gewinnen und zu verbrauchen, wäre diesem Ansatz tatsächlich kaum vorzuziehen.




Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.