Lexikon der Biochemie: Fettsäurebiosynthese
Fettsäurebiosynthese, ein Prozess, der durch die Fettsäure-Synthase katalysiert wird und bei dem die Fettsäurekohlenstoffkette schrittweise aus C2-Einheiten (die von Malonylgruppen stammen, mit anschließender Decarboxylierung) aufgebaut wird. Die Intermediate der Fettsäurebiosynthese sind Thioester des Acyl-Carrier-Proteins (ACP) und des Coenzyms A wie beim Fettsäureabbau.
Malonyl-CoA wird durch eine biotinabhängige Carboxylierung von Acetyl-CoA synthetisiert (Biotin):

Die Malonylgruppe von Malonyl-CoA wird auf das ACP übertragen, wo sie eine Thioesterbindung mit der SH-Gruppe des kovalent gebundenen 4-Phosphopantetheins eingeht. Dieser Phosphopantetheinarm dient als Träger für Substrate und Intermediate, die anschließend durch die anderen katalytischen Aktivitäten der Fettsäure-Synthase auf ihn übertragen werden (Tab. 1 und Tab. 2). Die Zick-Zack-Linie stellt den beweglichen Pantetheinarm des Acyl-Carrier-Proteins dar. Der mittlere Kreis repräsentiert das Acyl-Carrier-Protein und die äußeren Kreise die anderen Enzyme (Tab. 1). Die rein schematische Darstellung gibt nicht notwendigerweise die wirkliche Aneinanderreihung der Proteine wider. Jede neu gebildete gesättigte Acylgruppe wird vom Phosphopantetheinarm auf die SH-Gruppe eines Cysteinylrests ("periphere" SH-Gruppe) der β-Ketoacyl-Synthetase transferiert. Anschließend wird die nächste Malonylgruppe an das freigewordene zentrale Thiol gebunden und ein neuer Reaktionszyklus (Kondensation, Reduktion, Dehydratisierung, Reduktion) erweitert die Acylgruppe durch zwei weitere Kohlenstoffatome. Diese Zyklen werden wiederholt, bis ein Palmitoylrest (C16) entstanden ist, der dann entweder als freie Säure oder als Fettsäureacyl-CoA freigesetzt wird, abhängig davon, ob das System eine Thioesterase oder eine CoA-Transacylase (Tab. 2) besitzt. Für den Fall der Palmitatsynthese lautet die stöchiometrische Gleichung:
Acetyl-CoA + 7Malonyl-CoA + 14NADPH + 14H+ → Palmitat + 7CO2 + 14NADP+ + 8HSCoA + 6H2O.
Bei den meisten Bakterien und in den Chloroplasten sind das Acyl-Carrier-Protein und die Enzyme der Fettsäurebiosynthese diskrete Proteine, die in einem Multienzymkomplex (Typ-II-Fettsäure-Synthase) nichtkovalent assoziiert sind. Dagegen besteht die Fettsäure-Synthase bei Tieren (Typ I) aus einem Dimer eines einzelnen multifunktionellen Proteins. Die Fettsäure-Synthase der Hefe stellt einen Zwischentyp dar (Typ I/Typ II) (Tab. 2).
Bei Tieren läuft die Fettsäurebiosynthese im Cytoplasma ab. Die Startsubstanz, das Acetyl-CoA wird in den Mitochondrien mit Hilfe der Pyruvat-Dehydrogenase (Multienzymkomplex) produziert. Der Hauptweg für die Bereitstellung von cytosolischem Acetyl-CoA wird in Abb. 2 gezeigt.
Für jedes Acetyl-CoA, das von den Mitochondrien in das Cytosol transportiert wird, wird ein NADPH erzeugt. Bei der Umwandlung von 8 Molekülen Acetyl-CoA in Palmitat werden 8 der benötigten 14 NADPH-Moleküle durch die Malat-Dehydrogenase (EC 1.1.1.40, Abb. 2) zur Verfügung gestellt. Die restlichen 6 NADPH liefert der Pentosephosphat-Zyklus. Der geschwindigkeitsbestimmende Schritt in der Synthese von Fettsäuren aus Acetyl-CoA ist die Synthese von Malonyl-CoA, die durch die Acetyl-CoA-Carboxylase katalysiert wird. Die aktive Acetyl-CoA-Carboxylase aus tierischem Gewebe ist ein Polypeptid (Mr 4-8·106Da), das in inaktive Monomere oder Dimere der Mr 230 kDa-Untereinheit dissoziiert werden kann. Jede Untereinheit stellt ein multifunktionelles Protein dar, das die katalytischen Aktivitäten der Biotin-Carboxylase, des Biotin-Carboxy-Carrier-Proteins und der Transcarboxylase, sowie die regulatorische allosterische Bindungsstelle (Biotin) enthält. Citrat und Isocitrat aktivieren das Enzym, indem sie die Aggregation der Untereinheiten fördern. Der Antagonist des Citrateffekts ist Palmitoyl-CoA, das auch den Carrier inhibiert, der Citrat über die innere Mitochondrienmembran transportiert (Abb. 2).
Elongation der Fettsäurekohlenstoffkette. Die Spezifität der β-Ketoacyl-ACP-Synthase bewirkt, dass das Enzym normalerweise Fettsäuregruppen bis zu einer Kettenlänge von C14 (Tetradecanoylrest) bindet. Der Hexadecanoylrest (C16-, Palmitoylrest) kann nicht gebunden werden, so dass Palmitat bzw. Palmitoyl-CoA als Endprodukt der Fettsäurebiosynthese freigesetzt wird. Die Kettenlänge kann mit Hilfe von Elongationsreaktionen verlängert werden, die sich in den Mitochondrien und im endoplasmatischen Reticulum bei Tieren abspielen. In den Mitochondrien wird die Elongation durch Addition von Acetyl-CoA-Einheiten durchgeführt (nicht Malonyl-ACP). Dieser Weg gleicht beinah einer Umkehrung der β-Oxidation (Fettsäureabbau), mit dem Unterschied, dass die ungesättigte Bindung an C2 durch NADPH und nicht durch FADH2 reduziert wird. Im endoplasmatischen Reticulum stammen die C2-Einheiten für die Elongation vom Malonyl-CoA ab und alle Zwischenstufen liegen in Form ihrer CoA-Ester vor (ACP-Ester sind nicht beteiligt; Abb. 3). Das mikrosomale Elongationssystem ist möglicherweise physiologisch wichtiger als das mitochondriale System. Wahrscheinlich arbeitet das mitochondriale System nur, wenn das NADH/NAD+-Verhältnis in den Mitochondrien hoch ist, d. h. unter anaeroben Bedingungen bzw. in der Leber, wenn große Mengen an Ethanol oxidiert werden.
Bei Bakterien und Pflanzen läuft die Elongation durch Fortführung der Reaktionen der Fettsäurebiosynthese über C16 hinaus ab, wobei Synthasen unterschiedlicher Spezifität eingesetzt werden. Aus Pflanzen wurden zwei β-Ketoacyl-Synthasen isoliert. Die erste stellt primär Palmitat her, während die Produktverteilung in Gegenwart der zweiten Synthase in Richtung Stearat verschoben wird. Ungesättigte Säuren werden auf die gleiche Weise verlängert wie gesättigte. Zur Biosynthese ungesättigter Fettsäuren s. dort.
Synthese von Fettsäuren mit ungerader Kohlenstoffzahl und von Fettsäuren mit verzweigten Ketten. Durch die Einführung verschiedener Primer oder Startermoleküle in die Fettsäurebiosynthese anstelle von Acetyl-CoA entstehen ungeradzahlige oder verzweigte Kohlenstoffketten (Tab. 2).
, Reaktion 2).
Die Elongation der verzweigten Startermoleküle in Tab. 1, Reaktion 2).
führt zu verzweigten Fettsäuren, deren Verzweigung von der Carboxylgruppe entfernt liegt. Für die Synthese verzweigter Fettsäuren, mit einer Verzweigung in der Nähe der Carboxylgruppe, muss das Startermolekül unverzweigt sein und es muss in den letzten Schritten der Elongation ein verzweigtes Substrat, z. B. Methylmalonyl-CoA, eingeführt werden. Die Mycocerosinsäuren sind eine Familie multimethylverzweigter Säuren, die von Mycobakterien, wie etwa Mycobacterium tuberculosis-var. bovis Bacillus Calmette-Guérin hergestellt werden. Sie besitzen meistens eine gerade Kette aus 18-20 Kohlenstoffatomen und einen multimethylverzweigten Bereich am Carboxyende: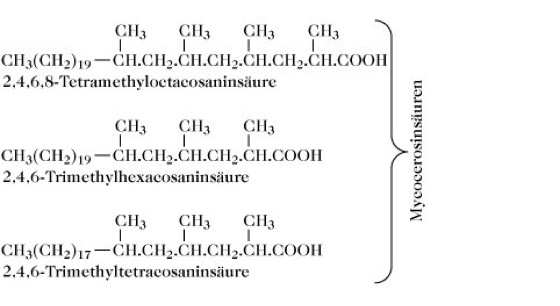
Aus Mycobacterium tuberculosis var. bovis BCG wurde eine neue Fettsäure-Synthase, die Mycocerosinsäure-Synthase isoliert, die n-Fettsäureacyl-CoA mit Methylmalonyl-CoA verlängert [D.L. Rainwater u. P.E. Kolattukudy J. Biol. Chem. 260 (1985) 216-223]. Sie besteht aus zwei identischen Untereinheiten (Mr Untereinheit 238kDa, Mr Dimer 490 kDa). Sie verlängert gerade Fettsäureacyl-CoA-Ester von n-C6 auf n-C20, unter Bildung der korrespondierenden tetramethylverzweigten Mycocerosinsäuren und verwendet kein Malonyl-CoA.
Verzweigungsmethylgruppen, die in der Nähe des Zentrums der Fettsäurekette liegen, rühren von einer Kohlenstoffübertragung von S-Adenosyl-L-methionin auf ein ungesättigtes Fettsäurederivat in einem Phospholipid her, gefolgt von einer Reduktion. Ein Beispiel hierfür ist die Synthese von 10-Methylstearinsäure (Tuberculostearinsäure) bei Mycobakterien, Nocardia, Streptomyces und Brevibacterium: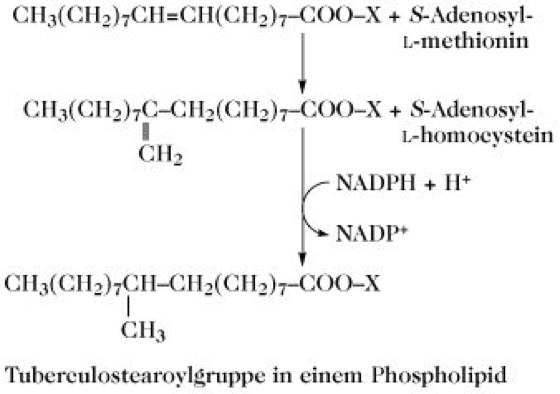
Cyclopropanfettsäuren (gramnegative Bakterien, einige grüne Pflanzen, Zooflagellate) werden durch eine Kohlenstoffübetragung von S-Adenosyl-L-methionin auf ein cis-einfachungesättigtes Fettsäurederivat gebildet:
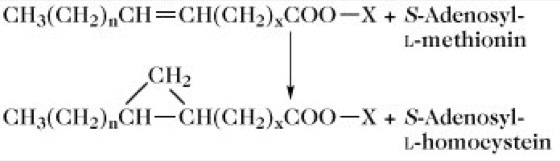
Hydroxyfettsäurenkönnen Intermediate der Fettsäurebiosynthese sein, die derivatisiert worden sind (3-Hydroxyfettsäuren mit D-Konfiguration). Sie können auch durch Oxygenierung, katalysiert durch Cytochrom-P-450-Systeme (insbesondere ω-Oxidation bei Eukaryonten; Fettsäureabbau), entstehen. Eine weitere Methode zur Biosynthese von Hydroxyfettsäuren ist die Hydratisierung von Doppelbindungen ungesättigter Fettsäuren. Spezifische Fettsäure-Hydratase-Systeme, die diese Reaktion katalysieren, wurden für Bakterien, insbesondere Pseudomonas-Arten, charakterisiert. [J.B. Ohlrogge Trends Biochem. Sci. 7 (1982) 386-387; J.S. Wakil et al. Annu. Rev. Biochem. 52 (1983) 537-579; A.J. Fulco Prog. Lipid Res. 22 (1983) 133-160; A.D. McCarthy u. D.G. Hardic Trends Biochem. Sci. 9 (1984) 60-63]

Tab. 1. Fettsäurebiosynthese. Reaktionen der Fettsäuresynthese. Das Enzym besitzt eine periphere SH-Gruppe (die zu einem Cysteinrest gehört) und eine zentrale SH-Gruppe (die zu Pantethein gehört). Mit Ausnahme der Acetyl-CoA-Carboxylase können die katalytischen Aktivitäten (zusammen mit dem Acyl-Carrier-Protein), die in der Tabelle aufgelistet sind, entweder Bestandteil diskreter Proteine in einem Multienzymkomplex sein oder sie sind alle in einem einzelnen multifunktionellen Protein vorhanden (s. Tab. 2).
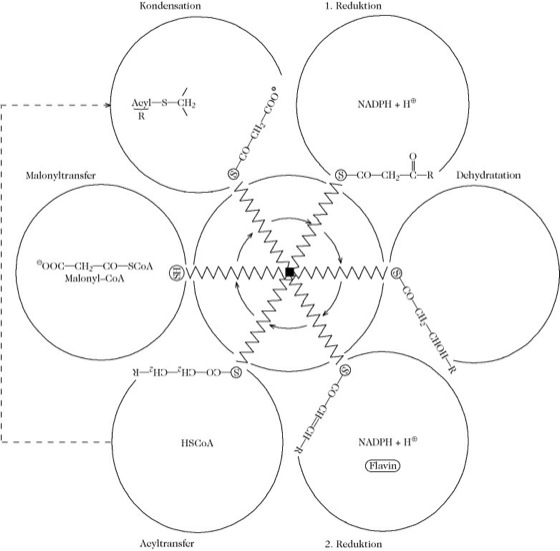
Abb. 1. Fettsäurebiosynthese. Kooperative Aktivität der Proteine der Fettsäure-Synthase, die als Multienzymkomplex bzw. als einzelnes multifunktionelles Protein vorliegen kann (Tab. 2). Die Zick-Zack-Linie stellt den beweglichen Pantetheinarm des Acyl-Carrier-Proteins dar. Der mittlere Kreis repräsentiert das Acyl-Carrier-Protein und die äußeren Kreise die anderen Enzyme (Tab. 2).
). Die rein schematische Darstellung gibt nicht notwendigerweise die wirkliche Aneinanderreihung der Proteine wider.
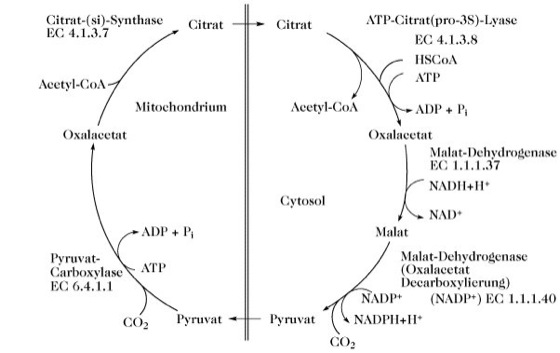
Abb. 2. Fettsäurebiosynthese. Produktion von cytosolischem Acetyl-CoA auf Kosten von mitochondrialem Acetyl-CoA durch Bildung, Transport und Abbau von Citrat.
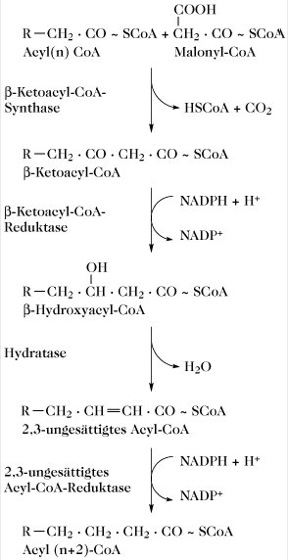
Abb. 3. Fettsäurebiosynthese. Das endoplasmatische Reticulum-System zur Elongation von Fettsäureacylketten.











Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.