Lexikon der Biochemie: Lignin
Lignin, Holzstoff, ein aus aromatischen Ringen bestehendes Polymerisat, das das Inkrustationsmaterial der Zellwand von Pflanzenzellen bildet und für deren Dicke und Stärke verantwortlich ist. Chemisch ist L. schlecht definierbar. Nach Freudenberg ist L. ein makromolekulares, irreversibles, verzweigtes Dehydrierungspolymerisat oder -kondensat mit übergeordneter additiver Verknüpfung. Nach Adler und Gierer ist L. die durch Säuren im wesentlichen nicht hydrolysierbare, polymorphe, amorphe, inkrustierende Substanz des Holzes, aufgebaut aus Methoxyl-haltigen Phenylpropaneinheiten, die durch Etherbindungen und C-C-Bindungen verknüpft sind. L. wird auch als "Zufallspolymer aus Hydroxyphenylpropaneinheiten" beschrieben. Bezüglich der chemischen Beschaffenheit von L. bestehen Speziesspezifitäten. Am besten untersucht ist das Fichtenholzlignin.
Biosynthese. Primäre Ligninbausteine sind Hydroxyzimtalkohole nach Art des Coniferyl-, Sinapin- und p-Cumarylalkohols. Das L. der Nadelhölzer wird vor allem aus Coniferylalkohol und wechselnden, stets kleinen Anteilen von Sinapin- und p-Cumarylalkohol aufgebaut. Das L. zweikeimblättriger Bedecktsamer, insbesondere der Laubhölzer, wird vor allem aus Sinapin- (~44%) und Coniferylalkohol (48%) gebildet, neben 8% p-Cumarylalkohol. Das L. von Gräsern setzt sich aus p-Cumaryl- (~30 %), Coniferyl- (~50 %) und Sinapyl- (~20 %) Alkohol zusammen. Diese primären Ligninbausteine werden aus den aromatischen Aminosäuren L-Phenylalanin und L-Tyrosin gebildet (Abb.). Die erste Reaktion wird durch L-Phenylalanin-Ammoniak-Lyase (EC 4.3.1.5) katalysiert. Dieses Enzym wird unter Beteiligung von Phytochrom durch Licht induziert und ist für die Synthese von pflanzlichen phenolischen Verbindungen aus Phenylalanin und Tyrosin von allgemeiner Bedeutung.
Der gesamte Vorgang der Biosynthese von L. ist ein Wechselspiel von enzymatischer Phenoldehydrierung und nichtenzymatischer Kupplung von Radikalen, die aus Phenolationen durch den Verlust eines Elektrons entstehen, und wird als reduktive Polymerisation (Dehydrierungspolymerisation) bezeichnet.
Der Vorgang kann im künstlichen Ligninverfahren bewiesen werden: Coniferylalkohol (80 mol%), p-Cumarylalkohol (14mol%) und Sinapylalkohol (6mol%) werden unter streng aeroben Bedingungen mit einer Phenol-Oxidase (z.B. der Pilz-Laccase) inkubiert. Das Produkt ist mit dem Fichtenlignin identisch. Vermutlich ist für die Ligninbiosynthese eine Peroxidase oder ein ähnliches Oxidationssystem verantwortlich.
Bei Anwendung der Isotopentechnik auf das Studium der Ligninbiosynthese müssen Ligninkriterien angewandt werden, da das markierte Reaktionsprodukt eindeutig gegen andere Zellwandpolymerisate analytisch abgegrenzt werden muss. Eine Methode besteht darin, das L. in situ abzubauen und anschließend Abbauprodukte zu isolieren, von denen zweifelsfrei bekannt ist, dass sie von L. abstammen. Beispielsweise zeigte Hibbert, dass das Erhitzen von Holz unter Rückfluss mit Ethanol, das 2% HCl enthält, ein Gemisch aus wasserlöslichen aromatischen Ketonen ergibt. Diese Verbindungen, die sog. Hibbertschen Ketone, haben folgende Strukturen: R-CO-CO-CH3, R-CH2-CO-CH3, R-CO-CH(OC2H5)-CH3 und R-CH(OC2H5)-CO-CH3, wobei R ein Guaiacyl- oder Syringylrest ist. Die Hibbertschen Ketone repräsentieren die intakte Phenylpropanstruktur der ursprünglichen L. [D. Fengel u. G. Wegener Wood – Chemistry, Ultrastructure, Reactions, DeGruyter, Berlin, New York, 1989; A.M. Boudet u. J. Grima-Pettenati Molecular Breeding2 (1996) 25-39]
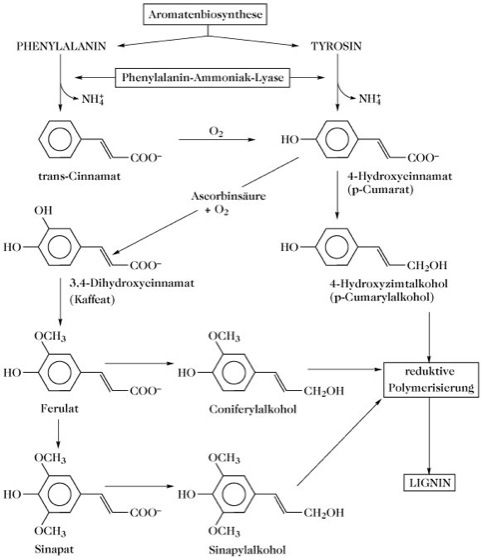
Lignin. Biosynthese von Lignin.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.