Lexikon der Biologie: Membranpotential
Membranpotentials [von *membran- , Potential], Bezeichnung für die zwischen dem Innern einer Zelle und der durch Membranen abgetrennten extrazellulären Flüssigkeit bestehende elektrische Potentialdifferenz (Potential). Die Ausbildung eines Membranpotentials ist eine Eigenschaft aller Zellen. Es besitzt eine wichtige Funktion bei vielen biologischen Prozessen. Besondere Bedeutung hat das Membranpotential für Nervenzellen, Muskelzellen (Muskeln, Muskulatur) und Sinneszellen. Bei diesen Zellen wird das Membranpotential als Ruhepotential bezeichnet. Infolge von Reizeinwirkungen (Erregung) treten bei den Zellen Spannungsänderungen auf, die vom Membran-Ruhepotential ausgehen und wieder zu diesem zurückkehren (Depolarisation). Diese Spannungsänderungen, die in Form elektrischer Impulse (Erregungsleitung, Nervenimpuls;Aktionspotential, Rezeptorpotential) entlang den Membranen geleitet werden, dienen der Informationsübertragung (Information) im Organismus und ermöglichen diesem sowohl die Kommunikation mit der Umwelt als auch eine Kommunikation einzelner Teile bzw. Organe des Organismus untereinander (Nervensystem). Die Höhe des Membranpotentials ist von Zelle zu Zelle verschieden und liegt in der Regel zwischen (–)50 mV und etwa (–)100 mV, wobei sich das Zellinnere negativ gegenüber der Außenseite verhält. Kleinere Membranpotentiale kommen nur bei glatten Muskelzellen (glatte Muskulatur) in einer Größenordnung von (–)30 mV vor. Das Membranpotential ist immer negativ und weist bei den einzelnen Zelltypen eine charakteristische, konstante Größe auf. Gemessen wird es mit Mikroelektroden, von denen die eine ins Zellinnere eingeführt wird, während sich die Referenzelektrode im extrazellulären Raum befindet ( vgl. Abb. 1 ). Die Ursachen des Membranpotentials sind ein Konzentrations-Gradient der Ionen über der Membran und deren selektive Permeabilität. Im Zellinnern befinden sich in hoher Konzentration Proteinmoleküle (Proteine), die bei einem Zell-pH-Wert von ca. 7,2 als Anionen vorliegen; des weiteren in ungefähr äquimolarer Konzentration positiv geladene (Kationen) K+-Ionen (Kalium) sowie in erheblich geringerer Konzentration Na+-, Cl–- und HCO3–-Ionen (Natrium, Chlor, Hydrogencarbonat). Völlig andere Verhältnisse herrschen dagegen in der extrazellulären Flüssigkeit: diese ist frei von Proteinmolekülen und weist hinsichtlich der anderen Ionen umgekehrte Verhältnisse auf, d.h. hohe Na+- und Cl–-Ionen-Konzentrationen und einen erheblich geringeren Anteil an K+- und HCO3–-Ionen ( vgl. Tab. 1 ). Im Ruhezustand sind die Membranen für Proteinmoleküle impermeabel, haben aber eine hohe Leitfähigkeit für K+-Ionen, eine in etwa um die Hälfte geringere Cl–-Ionen- und eine äußerst geringe Na+-Ionen-Leitfähigkeit. Die Permeabilitätskonstanten der 3 Ionenarten verhalten sich in etwa PK: PCl: PNa = 1 : 0,45 : 0,04. Diese Konstanten stellen zwar für einzelne Zellen feste Größen dar, können aber von Zelltyp zu Zelltyp stark variieren, wobei jedoch die Na+-Ionen-Leitfähigkeit die mit Abstand kleinste Größe ist. Infolge der hohen K+-Ionen-Konzentration im Innern der Zelle und der guten K+-Ionen-Leitfähigkeit der Membran sind die K+-Ionen bestrebt, einen Konzentrationsausgleich zwischen den beiden Reaktionsräumen herzustellen, und diffundieren in die extrazelluläre Flüssigkeit (Diffusion). Da die K+-Ionen Träger positiver Ladungen (elektrische Ladung) sind, werden deren elektrische Reaktionspartner, die negativ geladenen Proteinmoleküle, mitgezogen, bleiben aber, aufgrund der Impermeabilität der Membran für diese Moleküle, an deren Innenseite liegen. Beim Eintritt in die extrazelluläre Flüssigkeit werden die K+-Ionen von den ebenfalls positiv geladenen Na+-Ionen abgestoßen und an die Außenseite der Membran gedrängt, so daß diese innen eine hohe Dichte negativer und außen eine gleich hohe Konzentration positiver Ladungen aufweist. Aufgrund dieser Ladungsanordnungen können Membranen als Kondensatoren aufgefaßt werden ( vgl. Abb. 2 ). Diese Betrachtungsweise ermöglicht es, bei gemessenem Membranpotential und bekannter Membrandicke die erforderliche Menge an Ladungspaaren (innen gegenüber außen) pro Flächeneinheit quantitativ zu berechnen. Die Höhe des Membranruhepotentials ( vgl. Tab. 2 ), das sich aufgrund der oben dargelegten Diffusionsvorgänge an einer Membran einstellt, ist von der Konzentration der beteiligten Ionen abhängig. Die Diffusion der K+-Ionen aus dem Kompartiment mit hoher Konzentration (Zellinneres) dauert so lange an, bis das hierdurch aufgebaute elektrische Potential sich im Gleichgewicht mit dem Diffusionsbestreben der K+-Ionen befindet, d.h., bis die durch die K+-Ionen-Diffusion verrichtete osmotische Arbeit (Osmose) äquivalent ist der durch diese Diffusionsvorgänge – bei denen ja gleichzeitig elektrische Ladungen transportiert werden – erzeugten elektrischen Arbeit. Quantitativ lassen sich diese Verhältnisse mit der Nernstschen Gleichung
![]()
beschreiben (EK = Kalium-Gleichgewichtspotential, R = Gaskonstante = 8,314 J/(K · mol), T = absolute Temperatur, F = Faraday-Konstante = 96.487 C, [K+]a und [K+]i = K+-Ionen-Konzentration außen und innen). Da die Membranen nur für K+-Ionen frei permeabel sind, kann man das Membranpotential in erster Näherung als Kalium-Gleichgewichtspotential betrachten. Werden die aus dem Zellinnern und -äußern bestimmten Werte der K+-Ionen-Konzentration in die Nernstsche Gleichung eingesetzt und damit das Membranpotential errechnet, so ergeben sich zum gemessenen Membranpotential Differenzen von etwa 10 mV. Der Grund hierfür ist darin zu suchen, daß, wie an den Permeabilitätskonstanten ersichtlich, die Membranen für Cl–- und Na+-Ionen nicht völlig impermeabel sind. Eine nahezu vollständige Übereinstimmung in der Höhe des aus den Konzentrationsverhältnissen aller Ionen errechneten und tatsächlich gemessenen Membranpotentials ergibt sich, wenn die Nernstsche Gleichung um die Produkte aus den Permeabilitätskonstanten und den entsprechenden Ionen-Konzentrationen erweitert wird. Diese von V.A. Goldman, A.L. Hodgkin und B. Katz entwickelte Gleichung lautet:

(EM = Membranpotential, P = Permeabilitätskonstanten). – Lange Zeit nahm man an, das Membranpotential entspräche einem Donnan-Potential und ließe sich mit der Donnan-Gleichung berechnen. Eine Donnan-Verteilung und das daraus resultierende gleichnamige Potential stellt sich zwischen 2 durch eine semipermeable Membran getrennten Elektrolytlösungen (Elektrolyte) ein, wenn eine dieser Lösungen nicht diffusible Ionen enthält. Da aber semipermeable Membranen im Gegensatz zu biologischen Membranen für kleine Ionen gleichermaßen permeabel sind, stellen sich bei einer Donnan-Verteilung andere Konzentrationsverhältnisse und damit andere Potentiale ein. Errechnet man mit der Donnan-Gleichung z.B. das Membranpotential einer Froschmuskelzelle, so ergibt sich unter günstigsten Bedingungen ein Wert von –14 mV. Der tatsächlich gemessene Wert beträgt aber etwa –90 mV. Ein Donnan-Potential zwischen dem Zellinnern und -äußern kann demnach nur einen geringen Beitrag zum Membranpotential liefern. Der wesentliche Anteil muß durch die Membran selbst und deren selektive Permeabilitätseigenschaften verursacht sein. Ableitung, Adenosintriphosphat, Akkommodation, aktiver Transport, Alles-oder-Nichts-Gesetz, Bereitschaftspotential, Bioelektrizität, Biophysik, Chronobiologie, Diffusionspotential, Eccles (J.C.), elektrische Organe, elektrochemischer Gradient, Elektrotonus, Elektrophysiologie, Enzyme, erregendes postsynaptisches Potential, Fluoreszenz, Generatorpotential, Grenzflächen, hemmendes postsynaptisches Potential, Hodgkin-Huxley-Gleichungen, Huxley (A.F.), Hyperpolarisation, Ionenkanäle, Ionenpumpen, Membrantransport, Nachpotential, Natrium-Kalium-Pumpe, patch-clamp-Methode, Photorezeption, protonenmotorische Kraft, voltage-clamp-Methode; Nervenzelle I–II.
H.W.

Membranpotential
Abb. 1:Intrazelluläre Membranpotential-Messung.
1 Meßanordnung; die Zelle befindet sich in dem mit Plasma oder einer Ersatzlösung gefüllten Extrazellulärraum. a Meß- und Referenzelektrode liegen extrazellulär, Spannung zwischen beiden Elektroden Null; b Meßelektrode intrazellulär, Referenzelektrode extrazellulär, Spannungsmesser gibt das Ruhepotential an. 2 Potential vor und nach Einführen der Mikroelektrode in die Zelle.
Membranpotential
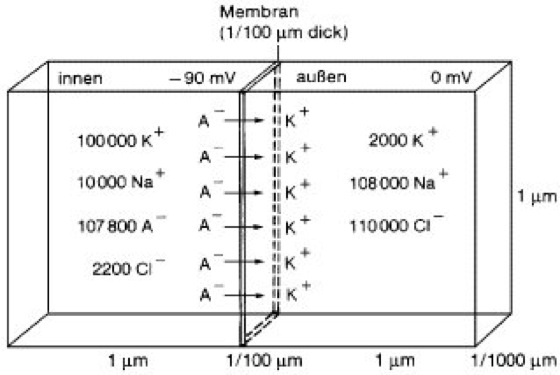
Abb. 2: Kondensatorfunktion der Membran – Membranladung beim Ruhepotential:
Darstellung eines sehr kleinen Membranstücks von 1 μm × 1/1000 μm Fläche und der angrenzenden intra- und extrazellulären Volumina von je 1 μm × 1 μm × 1/1000 μm Inhalt (angenommenes Membranpotential: –90 mV). Diese Membranfläche ist bei den angegebenen Ionenverteilungen von je 6 K+-Ionen und Anionen (A–) besetzt. Die Pfeile deuten die Diffusion der K+-Ionen durch die Membran aus der Zelle an. Angenommene Membrankapazität: 1 μF/cm2.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.