Individueller Geruch: Ein Hauch Genom in der Nase

Fragen Sie zehn Leute, wie man am besten den Partner fürs Leben findet, und Sie erhalten vermutlich zehn verschiedene Antworten. Und womöglich sind alle falsch. Denn wie jüngst ein Forscherteam um Theo Sturm von der Universität Tübingen herausfand, können Tiere die genetische Ähnlichkeit eines Artgenossen sehr präzise anhand erstaunlich niedrig konzentrierter Geruchstoffe bestimmen [1]. Der Schluss liegt nahe, dass sie diese Fähigkeit nutzen, um wichtige Informationen für ihre Partnerwahl oder andere Formen sozialer Interaktion zu sammeln.
Tiere sind freilich in vielerlei Hinsicht auf solche Informationen angewiesen. So müssen sie sich einen möglichst geeigneten Partner suchen, der jedoch gleichzeitig nicht zu nah mit ihnen verwandt sein darf, denn andernfalls besteht die Gefahr der Inzucht. Im Allgemeinen helfen ihnen verschiedenste Sinneskanäle bei der Lösung des Problems, wobei der Geruchssinn seit Langem im Mittelpunkt des Forschungsinteresses steht. Flüchtige chemische Verbindungen, die ein geeignetes Männchen oder Weibchen über große Distanzen anlocken, sind Paradebeispiele für diese Form der Kommunikation. Allerdings fehlt den so genannten Pheromonen die individuelle Komponente: Sie tragen allein art- und geschlechtsspezifische Information.
Hinweise auf die individuellen Eigenschaften eines möglichen Fortpflanzungspartners könnten sich stattdessen in den tausenden Varianten der Erbgutsequenz verbergen, über die sich selbst nah verwandte Angehörige ein und derselben Art unterscheiden lassen [2]. Dass Tiere tatsächlich diesen genetischen Kode in olfaktorische Information umsetzen können, scheint mittlerweile klar belegt zu sein [3, 4]. Doch erst langsam kommen Wissenschaftler dahinter, wie ihnen dies gelingt.
Die genetischen Unterschiede zwischen zwei Individuen manifestieren sich oft in einer veränderten Anordnung von Aminosäureresten in polymorphen, das heißt individuell verschiedenen Proteinen. Könnte es sein, dass diese Strukturunterschiede als eine Art "individuelle Signatur" nach außen durchscheinen? Dem ersten Anschein nach klingt das nicht plausibel, denn Proteine sind in der Regel zu groß, um beispielsweise als Geruchssignale über größere Entfernung zu wirken. Möglich ist allerdings, dass Proteine und Peptide – Bruchstücke, die bei ihrem Abbau entstehen – aus der Körperflüssigkeit zu Aerosolen zerstäubt werden und so einen direkten Zugang zur Nase des Gegenübers erhalten.
Zwei potenzielle Informationsträger liegen in der Luft
Um dies zu testen, haben Forscher an Mäusen untersucht, wie der Geruchssinn auf zwei Arten von Proteinen reagiert, deren genetische Bauanleitung von Individuum zu Individuum variiert: auf die Haupturinproteine (Major Urinary Proteins oder MUPs) [3], die in reichlicher Menge im Urin enthalten sind, und auf die Proteine des Haupthistokompatibilitätskomplexes (Major Histocompatibility Complex, MHC) [4], eines unverzichtbaren Bestandteils des Immunsystems vieler Tierarten. Ein Ergebnis dieser Untersuchungen war, dass sich Forscher nun uneins darüber sind, welche dieser beiden Proteinklassen die Hauptrolle bei den Individualitätssignalen der Maus spielt [5, 6].
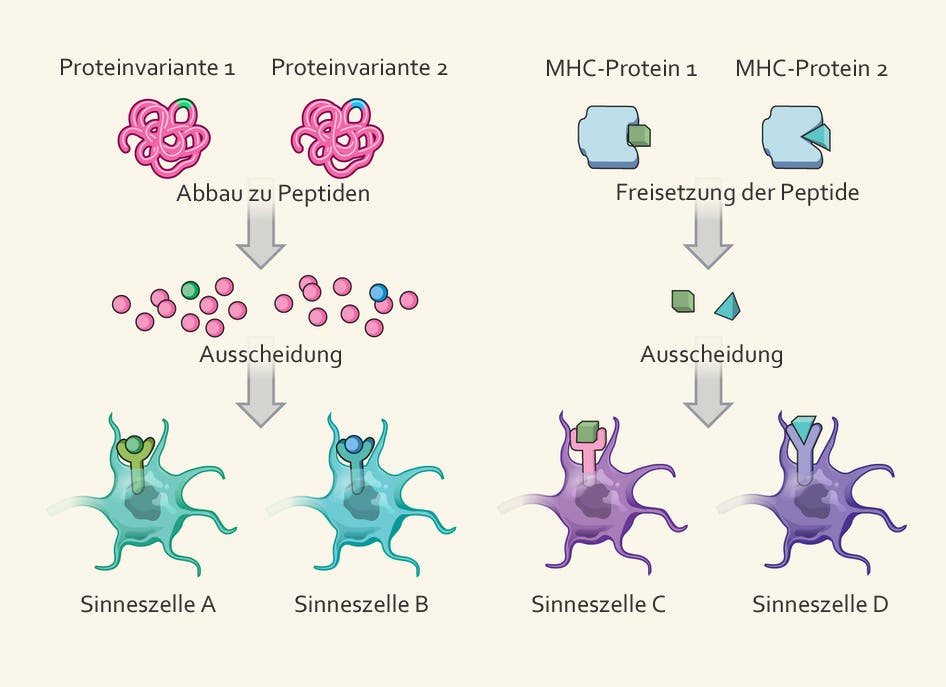
Strukturelle Unterschiede in den MUPs werden der allgemeinen Auffassung nach direkt vom olfaktorischen System detektiert [7], während der Aufbau von MHC-Molekülen nach Meinung einiger Forscher nur mittelbar erfasst werden kann [4], und zwar mit Hilfe ihrer Liganden, das heißt, über jene Substanzen, die an diese Proteine binden. Diese Liganden sind Abbauprodukte von intra- oder extrazellulären Proteinen und spiegeln in ihrer Form die Bindungseigenschaften der jeweiligen MHC-Moleküle wider – die Verknüpfung folgt dem weit verbreiteten Schlüssel-Schloss-Prinzip [8]. Die "MHC-Peptid-Hypothese" geht infolgedessen davon aus, dass Informationen über das Schloss (das MHC-Molekül) vermittels des Schlüssels (also des Peptids) gewonnen werden.
Dass Peptide schon in außergewöhnlich geringen Konzentrationen die Nervenzellen der Sinnesorgane erregen können, haben Wissenschaftler bereits vor einigen Jahren gezeigt [4]. Eine wichtige Vorhersage dieser Hypothese ist demnach erfüllt. Offen blieb allerdings, ob die entscheidenden Peptide überhaupt im Urin vorhanden sind. Um diese Lücke zu füllen, hat das Team um den Tübinger Theo Sturm nun mit Hilfe der Massenspektrometrie im Urin von Mäusen nach Peptiden gefahndet, von deren Sequenz sie annahmen, dass sie zu den MHC-Molekülen von Mäusen verschiedenen Genotyps passen.
Das "Peptidom" macht das Individuum
Obwohl sie auf eine Vielzahl solcher Moleküle stießen, machten sie die überraschende Entdeckung, dass deren Vorhandensein anscheinend unabhängig vom MHC-Genotyp des Tiers war. Allerdings zeigte sich auch: Markante genetische Unterschiede spiegelten sich nicht nur in den Haupturinproteinen, sondern auch in den Sequenzen einer Anzahl weiterer Urinpeptide wieder. Alles in allem scheint sich demnach die genetische Individualität eines Tieres am ehesten in der Gesamtheit seiner Urinpeptide, dem komplexen "Peptidom", zu manifestieren – zumindest zu einem gewissen Grad.
Warum aber ließen sich die erwarteten MHC-Liganden nicht so einfach dingfest machen? Vielleicht sei die Massenspektrometrie kein geeignetes Werkzeug dafür, überlegten Sturm und Kollegen. Die wenigen MHC-Ligandenpeptide könnten in der Masse millionenfach höher konzentrierter Urinpeptide schlicht untergehen. Als Umweg nutzten sie daher "leere" MHC-Proteine als Fänger für "freie" Ligandenpeptide im Mäuseurin. Das Ergebnis war eindeutig: Die MHC-Liganden waren in den Ausscheidungen der Nager vorhanden.
Im nächsten Schritt überprüften sie, wie einzelne Sinneszellen des Riechsystems auf MHC-unabhängige und -abhängige Peptide reagieren würden. Es zeigte sich, dass die Neurone die fraglichen Moleküle nicht nur bei biologisch relevanten Konzentrationen von 10-12 bis 10-6 Mol pro Liter erkennen, sondern darüber hinaus auch zwischen beiden Klassen zuverlässig unterscheiden können. Außerdem beobachteten Sturm und Kollegen, wie Cocktails aus Peptiden genetisch verschiedener Mäuse jeweils ganz eigene Aktivitätsmuster in den Nervenzellen auslösten. Es bietet sich also an, diese Peptidmischung tatsächlich als die gesuchte individuelle Signatur aufzufassen.
Unbekannte Hochleistungssensoren
Aus alldem lässt sich der Schluss ziehen, dass die beiden konkurrierenden Theorien, ob eher MUPs oder aber MHC-Liganden den entscheidenden Informationsträger darstellen, mitnichten so unvereinbar sind wie gedacht: Vielmehr scheint das jeweilige Aktivitätsmuster der Sinneszellen die unterschiedlichen Ursprünge der Peptide in ihrer gesamten Bandbreite wiederzugeben – seien es Liganden polymorpher MHC-Moleküle oder Abbauprodukte anderer polymorpher Proteine, womöglich auch MUPs.
Eine strukturelle Basis für diese Erkennungsleistung haben Forscher allerdings noch nicht ausfindig gemacht. Eine Möglichkeit für die Zelle wäre, an Stelle eines einzelnen Rezeptors so genannte heterooligomere Rezeptoren auszubilden. Sie bestehen aus verschiedenen Untereinheiten und könnten der Zelle die Fähigkeit verleihen, die diversen Peptide aufzuspüren.
Aus evolutionsbiologischer Perspektive deuten diese Erkenntnisse auf einen universellen Mechanismus hin, mit dem Tiere über ihr olfaktorisches System die genetische Individualität eines Artgenossen wahrnehmen, selbst wenn die Art gar nicht über einen MHC verfügt. Die Ergebnisse reichen in ihrer Tragweite jedoch über die reine Verhaltensforschung hinaus. Denn die außergewöhnliche Empfindlichkeit und Präzision, mit der Sinneszellen solche MHC-gebundenen Peptide erfassen, lässt es plausibel erscheinen, dass diese Fähigkeit auch zur Erkennung von Krankheitserregern eingesetzt wird. Immerhin entstehen die Peptide ja aus Bruchstücken dieser Erreger, die vermittels der MHC-Moleküle dem Immunsystem präsentiert werden und so am Ende in den Urin gelangen.
Eher praktisch denkende Menschen können sich hingegen über die Aussicht freuen, derart hochempfindliche Sinneszellen für Laborzwecke einsetzen zu können: als biologische Alternative zur herkömmlichen Massenspektroskopie. Das dürfte sich insbesondere dann lohnen, wenn es gilt, Peptidmischungen über einen großen Bereich von Konzentrationen zu analysieren.
Dieser Artikel erschien unter dem Titel "A whiff of genome" in Nature 304, S. 496-497, 2013





Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.