Lexikon der Chemie: Keto-Enol-Tautomerie
Keto-Enol-Tautomerie, chem. Gleichgewicht zwischen den Konstitutionsisomeren Keto-Form und Enol-Form, die bei Verbindungen mit dem Strukturelement R'-CO-CH2-R durch intramolekulare Wanderung eines Protons zwischen einem C-Atom und einem O-Atom bei gleichzeitiger Verschiebung einer Doppelbindung ineinander übergehen, z. B.
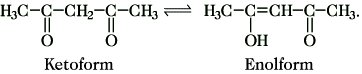
Die Lage des Gleichgewichtes wird vor allem durch die Stabilität der Tautomeren bestimmt. Die Enolisierungstendenz ist um so größer, je größer die CH-Acidität der Methylen- (Methyl-)Gruppe ist und je mehr das Enol durch Konjugation stabilisiert wird. Während bei Verbindungen des Typs R'-CO-CH2R das Gleichgewicht nahezu vollständig auf der Seite der Keto-Form liegt, ist es bei β-Dicarbonylverbindungen mehr oder weniger auf die Seite der Enol-Form verschoben. Äußere Faktoren, die die Lage des Keto-Enol-Gleichgewichtes bestimmen, sind die Art des Lösungsmittels und die Temperatur. Die Einstellung des Gleichgewichtes kann durch Säuren oder Basen katalysiert werden. Die Enol-Form läßt sich qualitativ in den meisten Fällen durch eine Eisen(III)-chloridreaktion (Rotfärbung) nachweisen, quantitativ mitunter durch Bromtitration (Bromaddition an die C=C-Doppelbindung). In besonderen Fällen, z. B. bei Acetessigester und Acetylaceton, lassen sich aufgrund der unterschiedlichen Löslichkeiten, Schmelz- und Siedepunkte die Keto- und die Enol-Form in reiner Form isolieren.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.