Astrochemie: Der Fingerabdruck der Kohlensäure
Auf der Erde kann freie Kohlensäure nicht existieren – sie zerfällt sofort wieder. Doch im kalten Weltraum oder in den Polkappen des Mars könnte sie stabil sein. Dank aktueller Entdeckungen österreichischer Forscher können Messinstrumente jetzt gezielt nach ihr suchen.

© Richard Zinken (Ausschnitt)

© spektrum.de (Ausschnitt)
Internationales Jahr der Chemie 2011
Kohlendioxid ist auch das, was im Sprudel sprudelt: Es steht zusammen mit Wasser im Gleichgewicht mit Hydrogenkarbonat und einem Proton, dass dem Getränk seine erfrischende Säure verleiht. Nur beim Übergang zwischen beiden Varianten taucht für einen extrem kurzen Moment die Struktur der freien Kohlensäure auf, um sofort wieder zu zerfallen. Sie ist ein Phantom.
Erst seit ein paar Jahren wissen wir, dass Kohlensäure auch länger als ein paar Sekundenbruchteile existieren kann. Wissenschaftler brachten Hydrogenkarbonat und Salzsäure eingefroren in winzige Methanoltröpfchen bei 78 Kelvin zusammen und erwärmten die Probe langsam, bis die gelösten Stoffe zueinander konnten. Auf diese Weise entstand tatsächlich die begehrte Säure, und Wissenschaftler konnten erstmals ihre Eigenschaften vermessen. Es gibt sie, so lange es nur kalt genug ist.
Damit stellte sich eine interessante Frage: Wie selten ist die Kohlensäure wirklich? Auch empfindliche Stoffe werden um so stabiler, je weiter die Temperatur absinkt. Kann sie möglicherweise auf anderen, kälteren Himmelskörpern oder im freien Weltraum als Gas existieren? Astrochemiker vermuten seit Langem, dass zum Beispiel Kometen freie Kohlensäure enthalten und an ihren Schweif abgeben können. Auch die Polkappen des Mars enthalten Wasser und Kohlendioxid in gefrorener Form. Verbinden sich die beiden dort auch zur Kohlensäure, die dann im Mars-Frühling verdampft?
© Lars Fischer (Ausschnitt)
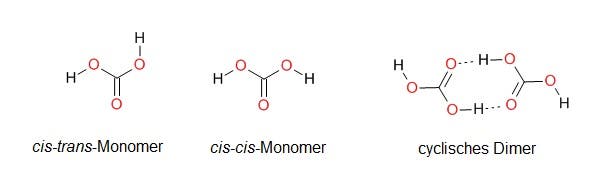
Freie Kohlensäure | In der Gasphase kommt freie Kohlensäure in drei sich ineinander umwandelnden Formen vor. Die häufigste Variante ist das cis-cis-Monomer, das unter den gemessenen Bedingungen zehn mal so häufig ist wie jede der beiden anderen Formen.
Jedes Molekül absorbiert durch seine Struktur eine ganz spezifische Kombination von bestimmten Wellenlängen, die bestimmte Teile des Moleküls zum Schwingen anregen. Dieses Spektrum identifiziert den Stoff nicht nur eindeutig, das Team stellte anhand seiner Feinheiten auch fest, dass Kohlensäure als Gas in drei verschiedenen Formen vorkommt: Die häufigste Form, das cis-cis-Konformer der Kohlensäure, kommt jeweils etwa zehn mal so häufig vor wie das cis-trans-Konformer und das cyclische Dimer aus zwei Molekülen Kohlensäure, das sich ebenfalls nachweisen ließ. Wichtiger jedoch ist, dass die Forscher damit endlich den Fingerabdruck der Kohlensäure kennen – und damit den so schwer fassbaren Stoff auch anderswo in Sonnensystem stellen können.



Schreiben Sie uns!
Beitrag schreiben