Tropenkrankheit: Gentechnisch manipulierte Mücken gegen Malaria
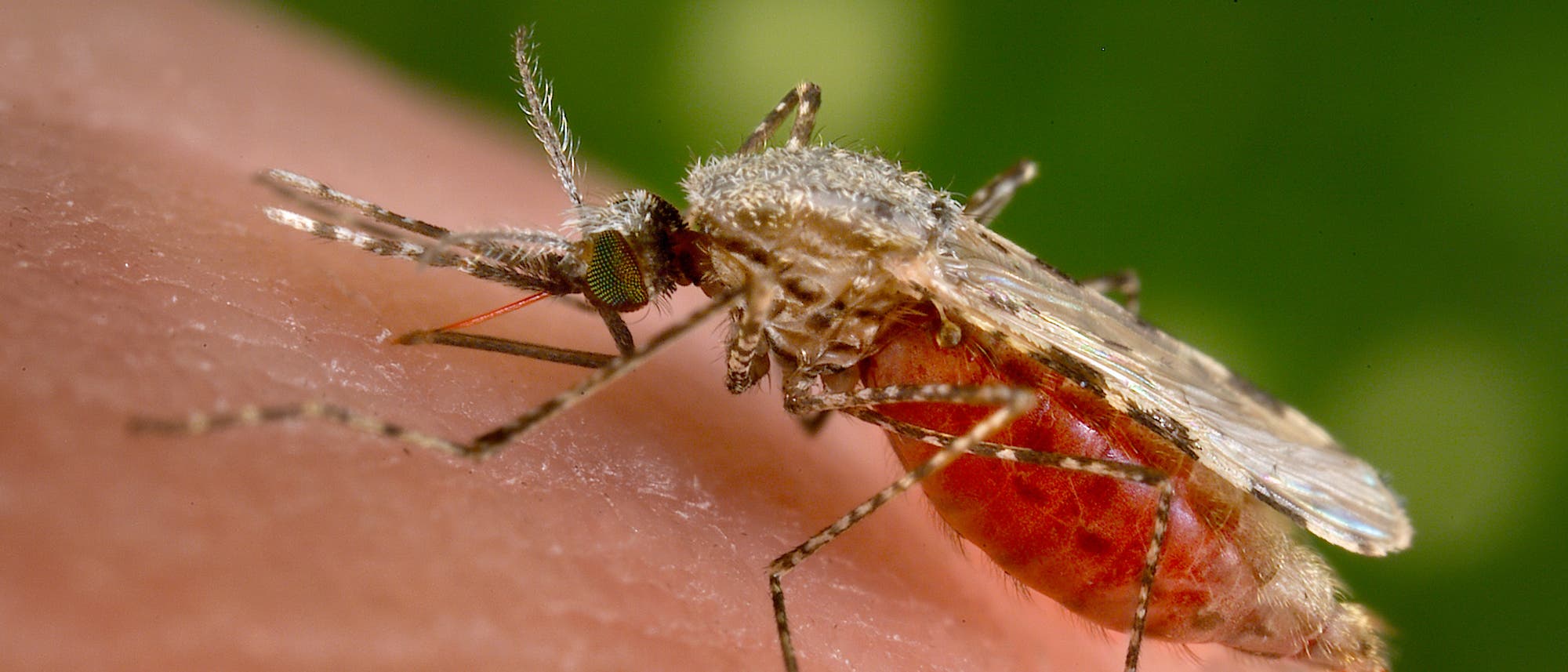
Die häufigste Tropenkrankheit wäre für immer besiegt, wenn man alle Mücken im Verbreitungsgebiet töten würde: Nur die Blutsauger übertragen die tödlichen Malariaerreger von Mensch zu Mensch. Selbst ein großflächiger Einsatz von umwelt- und gesundheitsschädlichen Insektiziden wie DDT, der vor Jahrzehnten zeitweise mancherorts durchexerziert wurde, hat dieses Ziel bei Weitem verfehlt. Später versuchten Forscher, Mücken gentechnisch gegen die Malariaparasiten resistent zu machen – mit noch geringerer Wirkung, weil eine freigesetzte und genmanipulierte Mückenpopulation sich nie gegen die vitaleren natürlichen Artgenossen durchsetzen konnte. Nun soll die neue Gentechnik-Wunderwaffe CRISPR Erfolg bringen: Mit der selbstreplizierenden Technik hoffen Forscher auf einen "Gene Drive", der die einmal eingekreuzten Resistenzgene in sämtliche Mücken und ihre Nachkommen bringt.
Erste Experimente verliefen nun viel versprechend: Forschern um Valentino Gantz von der University of California in San Diego brachten Malariaresistenzgene mit dem CRISPR-System in Mücken ein und konnten zeigen, dass diese Gene an fast alle Nachkommen der Insekten weitergegeben wurden. Im gentechnologischen Normalfall erbt statistisch nur die Hälfte der nächsten Mückengeneration eingeführte Resistenzgene: Sie integrieren sich nur in eine von zwei Chromosomenkopien, und der Zufall entscheidet, ob die Veränderung auch in die Keimzellen und damit die nächste Generation gelangt. CRISPR aber sorgt dafür, dass die Gene in beide Chromosomen gelangen und auch in rund 98 Prozent der Keimzellen, die dann nur die veränderte Variante enthalten. Dies ist die Grundlage für den erwünschten Gene Drive, also das rasche vollständige Ersetzen sämtlicher Zielgene in der Population durch die veränderte Variante.
Vergleichbare Versuche mit dem CRISPR-System und einer anderen Malariamückenspezies scheinen ähnlich erfolgreich zu verlaufen, beichtet "Nature News" vor der Veröffentlichung von Studiendaten. Die Erfolge dürften damit politisch und rechtlich schwierige Abwägungen provozieren: Tatsächlich würden mit den manipulierten malariaresistenten Mücken gentechnisch veränderte Organismen im Freiland ausgesetzt, deren neue Gene geradezu dafür gedacht sind, das Ökosystem und den Genpool zu verändern. Dabei ist etwa noch unklar, ob das genmanipulierte Erbgut auch auf andere Organismen übertragen werden kann – hierzu müssen noch Langzeitstudien unternommen werden. Als Vorsichtsmaßnahme haben zum Beispiel die Forscher in den USA daher zunächst nur die nicht einheimische indische Spezies Anopheles stephensi gentechnisch manipuliert. Selbst versehentlich freigesetzt würde sich diese Art außerhalb des Labors nicht halten können. In einem möglichen Feldversuch in den Malariagebieten soll allerdings später einmal das Gegenteil geschehen.


Schreiben Sie uns!
Beitrag schreiben