Lexikon der Chemie: Kugelpackung
Kugelpackung, räumliche Anordnung von starren Kugeln derselben Größe bei gegenseitiger Berührung von Nachbarkugeln. Das Modell der K. gestattet es, auf rein geometrischem Wege die Kristallstrukturen von Elementen, die aus Atomen aufgebaut sind (Metalle, Edelgase), wie auch von einfachen Ionensubstanzen abzuleiten und anschaulich zu beschreiben. Es hat sich gezeigt, daß vor allem K. mit hoher Packungsdichte und großer Koordinationszahl ausgebildet werden. Das primitive kubische Gitter mit 8 Kugeln an den Ecken der Elementarzelle weist die geringe Packungsdichte von 0,52 und die niedrige Koordinationszahl von 6 für jede Kugel auf, für das kubisch innenzentrierte Gitter ergeben sich die Werte 0,68 bzw. 8 (Abb. 1, Wolframtyp). Zu dichtesten K. gelangt man, wenn man von dichtest gepackten ebenen Kugelschichten ausgeht. Für diese gibt es nur eine mögliche geometrische Anordnung mit hexagonaler Symmetrie, bei der jede Kugel von 6 anderen sie berührenden Kugeln umgeben ist. Werden zwei derartige Schichten A und B so aufeinandergepackt, daß jede Kugel von A in eine Vertiefung zwischen je 3 Kugeln von B einrastet und umgekehrt, so entstehen zwischen den beiden Schichten zwei Arten von Hohlräumen unterschiedlicher Größe und Geometrie (Abb. 2): Tetraederlücken T sind von 3 Kugeln der einen und 1 Kugel der anderen Schicht, Oktaederlücken O dagegen von je 3 Kugeln aus der oberen und der unteren Schicht umgeben. Beträgt der Kugelradius r, so paßt in eine Tetraederlücke eine kleinere Kugel mit dem maximalen Radius 0,225·r, für eine Oktaederlücke darf der Radius der sie ausfüllenden Kugel nicht größer als 0,414·r sein.
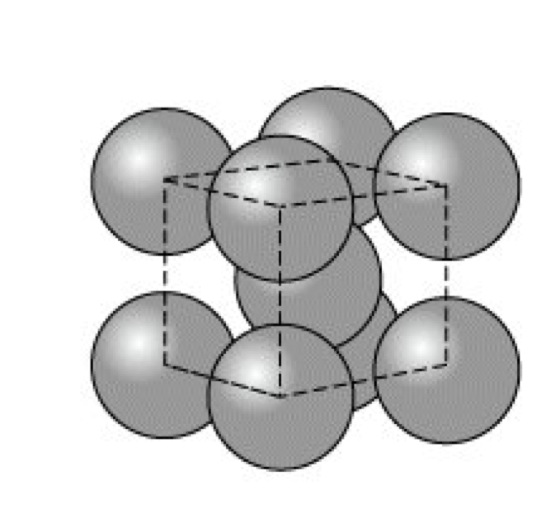
Kugelpackung. Abb. 1: Kubisch innenzentrierte Kugelpackung.

Kugelpackung. Abb. 2: Dichteste Kugelpackung zweier Schichten mit tetraedrischen Hohlräumen (T) und oktaedrischen Hohlräumen (O).
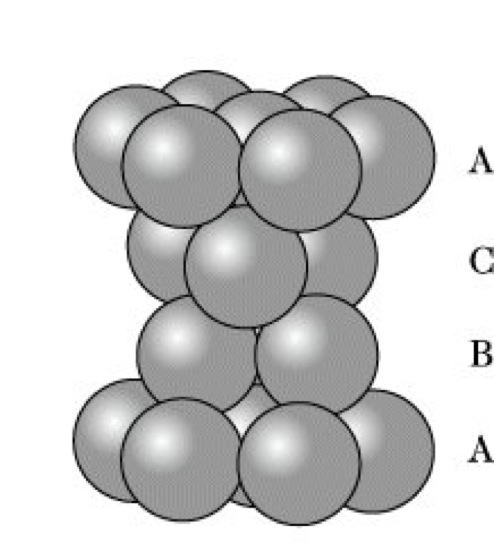
Für die Fortführung der Schichtstapelung gibt es zwei Möglichkeiten: 1) Die Kugeln der dritten Schicht liegen über denen der ersten Schicht, diese Schichtlage wird deshalb gleichfalls mit A bezeichnet. 2) Die Kugeln der dritten Schicht liegen über den Oktaederlücken, diese neue Schichtlage wird mit C bezeichnet. In beiden Fällen resultiert eine dichteste K. mit der Packungsdichte 0,74 und der Koordinationszahl 12 für jede Kugel. Von den bei weiterer Stapelung möglichen unendlich vielen dichtesten K. kommen die einfachsten besonders häufig vor: die hexagonal dichteste K. mit der periodischen Schichtfolge ABAB ... (Abb. 3, Magnesiumtyp) und die kubisch dichteste K. mit der Schichtfolge ABCABC ... (Abb. 4, Kupfertyp). Es treten aber auch kompliziertere dichteste K. (Polytypie), Störungen in der normalen Schichtfolge (Stapelfehler) und Strukturen mit statistisch regelloser Schichtfolge auf. Bezieht man die tetraedrischen und oktaedrischen Hohlräume als Gitterlücken, die von kleineren kugelförmigen Bausteinen besetzt werden können, in die Betrachtung ein, so läßt sich das Modell der K. auch mit Erfolg auf die Interpretation der Strukturen von Ionenkristallen anwenden.

Kugelpackung. Abb. 3: Schichtfolge ABAB ... der hexagonal dichtesten Kugelpackung.
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.