Lexikon der Biologie: Pharmakokinetik
Pharmakokinetikw [von *pharmako- , griech. kinētikos = bewegend, beweglich], Lehre der Konzentrationsverläufe von Arzneistoffen (Arzneimittel) und deren Metaboliten im tierischen und menschlichen Organismus. Die Pharmakokinetik beschreibt die zeitlichen Abläufe und die Transportprozesse eines Wirkstoffs als Folge der Applikation (Verabreichung), Resorption, Verteilung, Biotransformation und Ausscheidung ( vgl. Abb. 1 ). Ziel der Pharmakokinetik ist die Entwicklung der optimalen Arzneiformulierung, die Festlegung der Dosierungsvorschriften und die Gewinnung des Verständnisses vieler Wechselwirkungen und pharmakodynamischer Befunde (Pharmakodynamik). Unter den verschiedenen Formen der Verabreichung eines Arzneimittels ermöglicht die parenterale Applikation (d.h. unter Umgehung des Verdauungstrakts; meist intravenöse Injektion [in die Vene] oder Infusion) eine sehr exakte Dosierung, raschen Wirkungseintritt und eine vollständige Bioverfügbarkeit (s.u.). Am häufigsten ist die orale (durch den Mund) Applikationsform, da leicht herstellbar und vom Patienten bevorzugt; daneben intramuskuläre (in die Muskulatur), subkutane (unter die Haut), nasale (durch die Nase), rektale (durch den Mastdarm) und andere Dosierungen. Ausmaß und Geschwindigkeit der anschließenden Resorption im Organismus, d.h. der Aufnahme des Arzneistoffs in das Blutkreislaufsystem (Blutkreislauf), werden von verschiedenen Faktoren beeinflußt, wie physikalisch-chemische Eigenschaften des Arzneistoffs, Zusammensetzung der Arzneiform, Applikationsart, Milieu der resorbierenden Areale ( vgl. Abb. 2 ). Die Verteilung der Substanz vom Blutgefäßsystem in die Gewebebereiche und die nachfolgende Rück-Diffusion hängen u.a. von der Molekülgröße, der Löslichkeit und der Bindung an Plasma- (Serumproteine) und Gewebe-Proteine ab. Die quantitative Messung der Wirkstoffkonzentration im Blutplasma zu verschiedenen Zeitpunkten liefert charakteristische Plasmaspiegelkurven. Daraus lassen sich mit mathematischen Methoden pharmakokinetische Kenngrößen berechnen. Maximalspiegel und zugehöriger Zeitpunkt geben Aufschluß über den Verlauf der Resorption. Die Halbwertszeit gibt die benötigte Zeit an, in der die Hälfte der momentan im Organismus vorhandenen Arzneistoffmenge eliminiert (ausgeschieden) wird. Die Clearance umfaßt alle Eliminationsvorgänge des Wirkstoffs aus dem Organismus und stellt (bildhaft) die Flüssigkeitsmenge (z.B. Plasma) dar, die pro Zeiteinheit von Wirkstoff befreit wird. Mit Hilfe der Flächen unter den Plasmaspiegelkurven ( vgl. Abb. 3 ) als relatives Maß für die insgesamt in den Organismus gelangte Substanzmenge kann nach Applikation unterschiedlicher Arzneiformen die Bioverfügbarkeit berechnet werden. Dies ist von Bedeutung auch für den Vergleich verschiedener Arzneimittel am Markt mit gleicher Wirkstoffzusammensetzung (Bioäquivalenz). Weitergehende Auswertungen werden mit komplexeren pharmakokinetischen Berechnungen vorgenommen (Kompartiment-Modell). Die Biotransformation(Metabolismus) zu hydrophileren, leichter ausscheidbaren Stoffen erfolgt überwiegend in der Leber. Dabei finden im wesentlichen enzymatisch gesteuerte Oxidationen, Reduktionen, Hydrolysen und Konjugationen statt. Falls ein erheblicher Anteil des Wirkstoffs schon in der ersten Leberpassage metabolisiert wird und deshalb die systemische Blutzirkulation nie intakt erreicht, hat dieser Wirkstoff trotz weitgehender Resorption eine geringe absolute Bioverfügbarkeit (First-pass-Effekt). Bei wiederholter Gabe insbesondere gut lipidlöslicher Verbindungen mit langer Verweildauer in der Leber kann es zu vermehrter Enzymbildung mit erhöhter Biotransformation kommen (Enzym-Induktion; Gegensatz Enzyminhibition). Durch die Ausscheidung (Exkretion) werden Arzneistoff und seine Metaboliten endgültig aus dem Körper eliminiert. In Abhängigkeit von den physikalisch-chemischen Eigenschaften (relative Molekülmasse, pKa-Wert (pK-Wert), Löslichkeit, Dampfdruck) der auszuscheidenden Substanz erfolgt dies renal (Urin; Harn, Harnkonzentrierung, Niere), biliär und intestinal (Fäzes; Defäkation, Fäkalien) oder pulmonal (Atemluft; Atmung, Blutgase; Atmungsorgane I ). – Zahlreiche individuelle Faktoren der verschiedenen Patienten können die Pharmakokinetik eines Arzneimittels beeinflussen. Die gleiche Dosis kann bei verschiedenen Patienten zu unterschiedlichen Plasmaspiegelkurven führen. Beeinflussende Faktoren sind z.B. Lebensalter, Körpergewicht, genetische Differenzen, Rauchgewohnheiten (Rauchen), Nahrungsaufnahme (Ernährung), Alkohol (Ethanol) und Wechselwirkungen mit anderen Medikamenten (Arzneimittelwechselwirkungen). Bei Krankheiten wie Niereninsuffizienz und häufig im Alter mit verringerter Nierenleistung (Altern) ist die Eliminationsrate vieler Wirkstoffe reduziert und damit die Halbwertszeit erhöht. Hierbei ist ein mögliches Kumulationsrisiko zu berücksichtigen und bei Mehrfachgabe ( vgl. Abb. 4 ) gegebenenfalls das Dosierungsschema anzupassen. Bei eingeschränkter Leberfunktion kann die Metabolisierung gestört sein. Auch intraindividuelle Schwankungen treten auf, bedingt z.B. durch die Tageszeit (sog. Chronopharmakokinetik). Chronobiologie, Chronopharmakologie, endoplasmatisches ReticulumEntgiftung, molecular modeling, Nebenwirkungen, Stoffwechsel.
M.N.

Pharmakokinetik
Abb. 1: Pharmakokinetisches Verlaufsschema eines Arzneistoffs im Organismus
Pharmakokinetik
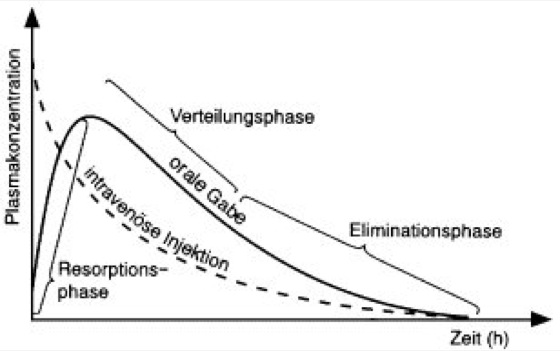
Abb. 2: Plasmaspiegelkurven eines Wirkstoffs nach intravenöser Injektion und oraler Gabe eines Arzneimittels mit Kennzeichnung der unterschiedlichen Phasen im Organismus
Pharmakokinetik
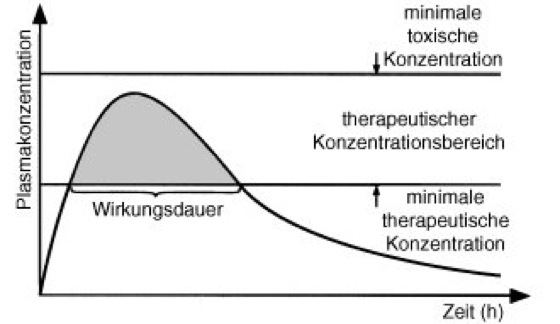
Abb. 3: Plasmaspiegelkurve eines Arzneistoffs in Beziehung zur therapeutischen Wirkung
Pharmakokinetik
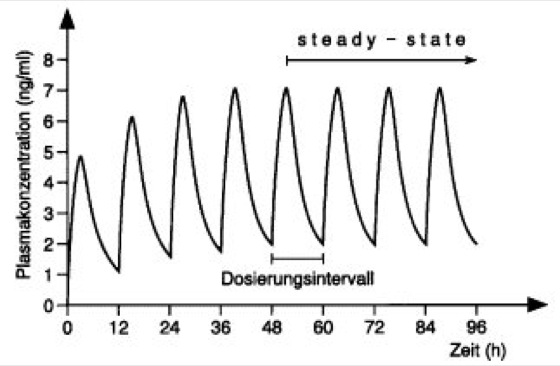
Abb. 4: Zunahme der Wirkstoffkonzentration und Erreichen des steady-state (Fließgleichgewichts) nach mehrfacher oraler Gabe eines Arzneimittels (2mal täglich)
Wenn Sie inhaltliche Anmerkungen zu diesem Artikel haben, können Sie die Redaktion per E-Mail informieren. Wir lesen Ihre Zuschrift, bitten jedoch um Verständnis, dass wir nicht jede beantworten können.