Lexikon der Chemie: Hochleistungsflüssigchromatographie
Hochleistungsflüssigchromatographie, Abk. HPLC (engl. high performance liquid chromatography), Hochdruckflüssigchromatographie, schnelle Flüssigchromatographie, Methode der Flüssigchromatographie unter optimierten Bedingungen durch Verkleinerung der Teilchengröße der stationären Phase auf 5 bis 10 μm (Abb. 1; vgl. Chromatographie). Bei idealen Säulen ist die Trennstufenhöhe gleich dem Teilchendurchmesser, mit industriell gefertigten Säulen erreicht man dreifache Werte. Die H. hat sich aus der Säulenchromatographie entwickelt und unterscheidet sich von dieser durch größere Analysengeschwindigkeit, höhere Trennleistung sowie eine Verkleinerung der Nachweisgrenze.
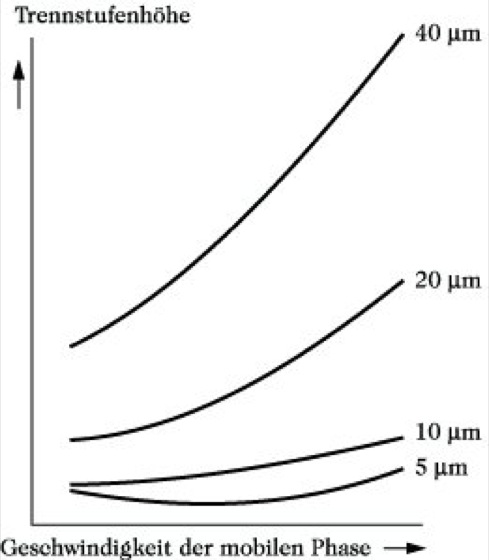
Hochleistungsflüssigchromatographie. Abb. 1: van-Deemter-Kurven.

Hochleistungsflüssigchromatographie. Abb. 2: Baugruppen eines HPLC-Gerätes: 1 Lösungsmittelvorratsgefäß, 2 Hochdruckpumpe, 3 Probendosiersystem, 4 Trennsäule, 5 Detektor, 6 Probensammler, 7 Datenauswertesystem.
Als Pumpen verwendet man Kurzhubkolbenpumpen, Kolbenmembranpumpen oder Langhubkolbenpumpen mit Fördervolumina von 0,1 bis 10 ml min-1 bei Drücken bis zu 60 MPa. Die Pumpen sollen eine möglichst pulsfreie Förderung des Eluenten und eine konstante Förderleistung garantieren. Große Bedeutung hat die Gradientenelution (binäre oder ternäre Gradienten), die entweder auf der Niederdruckseite durch Mischkammern oder auf der Hochdruckseite durch weitere Pumpen erfolgt. Die Probeninjektion kann im Niederdruckbereich durch Septuminjektion oder bei hohem Säulenvordruck mit Probenschleifen vorgenommen werden. Eine drucklose Probendosierung bei unterbrochenem Eluentenstrom ist die "stop flow"-Probenaufgabe.
Als Trennsäule verwendet man Edelstahlsäulen oder für niedere Drücke Glassäulen mit einem Innendurchmesser zwischen 2 und 4 mm und Längen von 10 bis 50 cm.
Der Detektor hat die Aufgabe, im Säuleneluat durch kontinuierliche Messung einer physikalischen Größe für die im Eluat enthaltenen Substanzen ein konzentrationsproportionales Meßsignal zu erzeugen. Zur Messung durchströmt das Eluat eine Durchflußzelle, deren Volumen zwischen 5 und 20 μl liegt. Die am häufigsten benutzten Detektoren sind der UV-Detektor (Empfindlichkeit 10-10 g ml-1) und das Differentialrefraktometer (Empfindlichkeit 10-7 g ml-1).
Die Lösungs- oder Elutionsmittel unterscheiden sich in der Lösungsmittelstärke, ihren Dielektrizitätskonstanten, der Viskosität und im Brechungsindex. Der Einsatz eines Eluenten richtet sich nach dem jeweiligen Trennproblem sowie dem verwendeten Trennprinzip. Zur Adsorptionschromatographie an polaren Adsorbenzien (Kieselgel, Aluminiumoxid) verwendet man unpolare oder wenig polare Lösungsmittel (Hexan, Methylenchlorid), an unpolaren Phasen (Umkehrphasen) polare Lösungsmittel (Wasser, Methanol). Im Falle der Verteilungschromatographie muß das Elutionsmittel mit der Trennflüssigkeit gesättigt sein. Zur Auswahl mobiler Phasen für spezielle Trennprobleme wurden eluotrope Reihen von Lösungsmitteln aufgestellt, die sich für hydrophile und hydrophobe Adsorbenzien unterscheiden (Tab. 1). Für viele Trennprobleme benötigt man Lösungsmittelgemische. Zur optimalen Auftrennung sehr komplexer Substratgemische verändert man programmiert die Elutionskraft der mobilen Phase (Gradient-Technik).
Hochleistungflüssigchromatographie. Tab.: Eluotrope Reihen von Lösungsmitteln für die Hochleistungsflüssigchromatographie.
| ||
| Adsorbenzien | ||
| Wasser | Hexan | |
| Methanol | Benzol | |
| Elutionskraft Ethanol | Essigsäureethylester | |
| Propan-1-ol | Diethylether | |
| Essigsäureethylester | Propan-1-ol | |
| Aceton | Aceton | |
| Diethylether | Ethanol | |
| Benzol | Methanol | |
| Hexan | Wasser |
Als Trägermaterialien verwendet man poröse Materialien (Kieselgel, Aluminiumoxid) mit großer spezifischer Oberfläche oder Dünnschichtteilchen (engl. porous layer beads, Abk. PLB) mit einer porösen Schicht (1 bis 3 μm) auf einem harten und undurchlässigen Kern (Glas). Durch Umsetzung der Silanolgruppen des Kieselgels mit organischen bzw. siliciumorganischen Verbindungen erhält man chemisch modifizierte Träger. Der organische Rest ist kovalent an die Trägeroberfläche gebunden, wobei man mit Alkylsilanen mit C2- bis C18-Kohlenstoffatomen ohne funktionelle Gruppen unpolare stationäre Phasen für die Umkehrphasenchromatographie, Abk. RPC (engl. reversed phase chromatography) erhält. Meist werden C8- und C18-Phasen verwendet (z. B. poröse Träger Lichrosorb RP 8 und RP 18 oder PLB Perisorb RP 8 und RP 18). Die H. kann als Adsorptions-, Verteilungs-, Ionenaustausch-, Permeations- oder Affinitätschromatographie betrieben werden. Die Methode findet breite Anwendung in allen Bereichen der Chemie, Biochemie und Pharmazie (Abb. 3).

Schreiben Sie uns!